Микробная колонизация на интерфейсе имплант-абатмент и ее возможное влияние на периимплантит: систематический обзор и мета-анализ
Машинный перевод
Оригинальная статья написана на языке EN (ссылка для ознакомления) .
Аннотация
Цель: Целью данного систематического обзора и метаанализа было оценить микробную колонизацию на интерфейсах имплант-абатмент (IAI) на имплантатах уровня кости и выявить возможную связь с периимплантными состояниями.
Выбор исследований: Основной вопрос заключался в том, связаны ли двухкомпонентные остеоинтегрированные имплантаты, находящиеся в эксплуатации не менее 1 года, у человека, с более высоким количеством бактерий и началом периимплантита по сравнению со здоровыми периимплантными состояниями. Стратегия поиска охватывала онлайн-литературу (MedLine, Google scholar, Cochrane library) с 1990 года до марта 2015 года, опубликованную на английском языке, с использованием комбинаций MeSH (медицинские предметные заголовки) и поисковых терминов. Оценка качества выбранных статей полного текста проводилась в соответствии с рекомендациями ARRIVE и CONSORT. Для анализа данных был рассчитан общий бактериальный счет Porphyromonas gingivalis, Tannerella forsythia, Treponema denticola, Prevotella intermedia и Fusobacterium nucleatum и сравнен с IAI с или без периимплантной патологии.
Результаты: Всего 14 статей, в которых представлены данные по 1126 имплантатам, соответствовали критериям включения и были подвергнуты оценке качества. Выбранные исследования показали загрязнение интерфейса имплант-абатмент (ИАИ) у пациентов, получивших двухкомпонентные имплантационные системы. Метанализ показал значительную разницу в общем количестве бактерий между имплантатами, пораженными периимплантитом, и здоровыми периимплантными тканями (0.387 0.055; 95% ДИ 0.279–0.496). Меньшее количество бактерий было выявлено в здоровом ИАИ для всех исследованных грамотрицательных бактерий, кроме T. forsythia.
Введение
Микротрещины на интерфейсе имплант-абатмент (ИАИ) характерны для двухкомпонентных остеоинтегрированных стоматологических имплантационных систем и, похоже, играют значительную роль в бактериальной колонизации в периимплантной бороздке. Это, в свою очередь, может привести к периимплантным воспалительным реакциям и, впоследствии, к потере поддерживающей кости. Бактериальная утечка на ИАИ вместе с узлами крепления абатмента, которые действуют как бактериальный резервуар, может вызвать ответ организма с воспаленными мягкими тканями и возможной маргинальной потерей периимплантной кости.
Бактериальная колонизация зазора в IAI также была связана с установлением физиологической биологической ширины. Основная часть потери краевой кости была зафиксирована в течение первого года после установки имплантата, после чего, у пациентов с адекватным уровнем гигиены полости рта, уровни краевой кости стабилизировались на протяжении многих лет. Микропроницаемость зазора между имплантатом и абатментом может позволять проход кислот, ферментов, бактерий и/или их метаболических продуктов, которые непосредственно влияют на периодонтальные ткани, вызывая кровотечения, отеки и запах. Тем не менее, соединения с конусом Морса, как предполагается, имеют более низкие уровни микропроницаемости и потери краевой кости по сравнению с имплантатами с внешним соединением.
Недавний обзор литературы описал Porphyromonas gingivalis, Treponema denticola и Tannerella forsythia, найденные в образцах субгингивальной биопленки, как микроорганизмы, имеющие умеренные доказательства связи с началом периимплантита. Напротив, только некоторые доказательства были найдены для Prevotella intermedia и Campylobacter rectus. В анаэробных условиях, подобных тем, что присутствуют внутри IAI, микробиологические показатели могут быть ответственны за отбор, в средне-долгосрочной перспективе, микробиологических видов, способных инициировать процесс периимплантита.
Целями данного систематического обзора и мета-анализа были оценка микробиологической колонизации на интерфейсе имплант-абатмент на двухкомпонентных имплантах уровня кости, независимо от конфигурации соединения, и исследование того, связано ли это с началом периимплантита.
Выбор исследования
Этот систематический обзор соответствует Руководящим принципам по предпочтительным отчетным элементам для систематических обзоров и мета-анализов (PRISMA) (http://www.prisma-statement.org). Протокол этого систематического обзора был опубликован в международном проспективном реестре систематических обзоров (PROSPERO, http://www.crd.york.ac.uk/PROSPERO/) с регистрационным номером CRD42016037481. Основной вопрос обзора заключался в том, существует ли связь между наличием более высокого бактериального счета и началом периимплантита по сравнению со здоровыми периимплантными условиями у пациентов с двухкомпонентными оссеоинтегрированными имплантами после как минимум 1 года функционирования. Периимплантит определялся по наличию глубины зондирования периимпланта ≥5 мм, связанной с кровотечением при зондировании и/или гнойным выделением, а также по рентгенографическим изображениям потери кости ≥3 мм по сравнению с первоначальными рентгенограммами при доставке протезной реставрации.
2.1. Источники информации
Искались статьи, опубликованные только на английском языке, которые сообщали о микробной колонизации на IAI и ее связи с началом периимплантита, опубликованные с 1990 года до марта 2015 года в базе данных PubMed Национальной библиотеки медицины США (http://www.ncbi.nlm.nih.gov/pubmed/), Google Scholar (http://www.google.com) и библиотеке Кохрейна (http://www.cochranelibrary.com/). Кроме того, ссылки на включенные статьи были проверены вручную для поиска дополнительных статей.
2.2. Стратегия поиска
Изначально вопрос PICOS (Популяция (P), Интервенция (I), Сравнение (C), Результаты и Дизайн исследования (O), Тип исследования (S)) определил стратегию поиска, где P=Двухкомпонентные остеоинтегрированные имплантаты с диагнозом периимплантит после как минимум 1 года функционирования; I=Микробная колонизация на IAI; C=Здоровые периимплантные условия; O=Уровень выживаемости; S=Случайные контролируемые клинические испытания (RCT) и клинические исследования с последующим наблюдением.
Электронные базы данных были исследованы с использованием комбинаций терминов MeSH (Медицинские предметные заголовки), поисковых терминов и их комбинаций: “дентальные имплантаты” [MeSH] И “бактериальное загрязнение” ИЛИ “наличие бактерии” ИЛИ “дентальная утечка/микробиология” [MeSH] ИЛИ “микроутечка” ИЛИ “микробиологические находки” ИЛИ “микробиологическая колонизация” ИЛИ “микробиота” ИЛИ “периимплантная микрофлора” И “периимплантит” [MeSH] ИЛИ “периимплантная патология” ИЛИ “периимплантное заболевание” И “Дентальные абатменты*/микробиология” [MeSH] “соединение, имплантат-абатмент” ИЛИ “дизайн абатмента дентального имплантата” [MeSH] ИЛИ “соединение имплантат-абатмент” ИЛИ “микрозазор имплантат-абатмент” ИЛИ “внутреннее пространство дентальных имплантатов” ИЛИ “внутренняя часть дентальных имплантатов”.
2.3. Выбор исследования и критерии приемлемости
Все заголовки и аннотации выбранных исследований сначала оценивались по следующим критериям включения: (1) Статьи, написанные на английском языке; (2) исследования с клиническим обследованием пациентов; (3) исследования, оценивающие количество различных бактериальных видов (бактериальное количество, BC) на уровне IAI у пациентов, получивших двухступенчатые имплантационные системы на уровне кости, независимо от конфигурации соединения; (4) Рандомизированные контролируемые клинические испытания (RCT), проспективные когортные исследования или поперечные исследования, сообщающие о функционирующих имплантатах в течение как минимум 1 года.
После оценки полного текста статей в соответствии с ранее определенными критериями исключения, статьи с следующими характеристиками, без ограничений по языкам, не были признаны подходящими: (a) Письма, нарративные или исторические обзоры; (2) исследования на животных и in vitro; (3) Отчеты о локально или системно скомпрометированных участках и/или состояниях (т.е. значительный костный дефект перед имплантацией, костные патологии, радиотерапия головы и шеи, лечение бисфосфонатами); (4) отчеты о пациентах, которые получили механическую дебридемию в предыдущие 3 месяца или антибиотики за последние 6 месяцев до анализа.
2.4. Процесс сбора данных
Два откалиброванных рецензента (М.Ч. и Л.Ч.) отобрали и собрали данные из выбранных статей в структурированные таблицы. Значения коэффициента Каппа Коэна между экзаменаторами были рассчитаны как на первом, так и на втором этапе исследования. Несоответствия были разрешены путем консенсуса, и был привлечен третий экзаменатор (М.Т.).
Статьи без аннотаций, но с заголовками, связанными с целями данного обзора, были отобраны, и их полный текст был проверен на соответствие критериям. Списки литературы отобранных статей были дополнительно проверены на наличие возможных дополнительных публикаций. Кроме того, были проведены ручные поиски в библиографиях выбранных систематических обзоров, ограниченные следующими журналами: Clinical Implant Dentistry and Related Research; Clinical Oral Implants Research; International Journal of Oral and Maxillofacial Implants; Journal of Clinical Periodontology; Journal of Periodontology.
2.5. Оценка качества, гетерогенности и риска смещения отдельных исследований
Одни и те же рецензенты оценивали риск смещения в включенной выборке в соответствии с рекомендациями, представленными в заявлении CONSORT для оценки рандомизированных контролируемых испытаний (http://www.consort-statement.org), заявлением STROBE для наблюдательных исследований (http://www.strobe-statement.org), а также модифицированными пунктами из Инструмента сотрудничества Кокрейна для оценки риска смещения (Таблица 1).
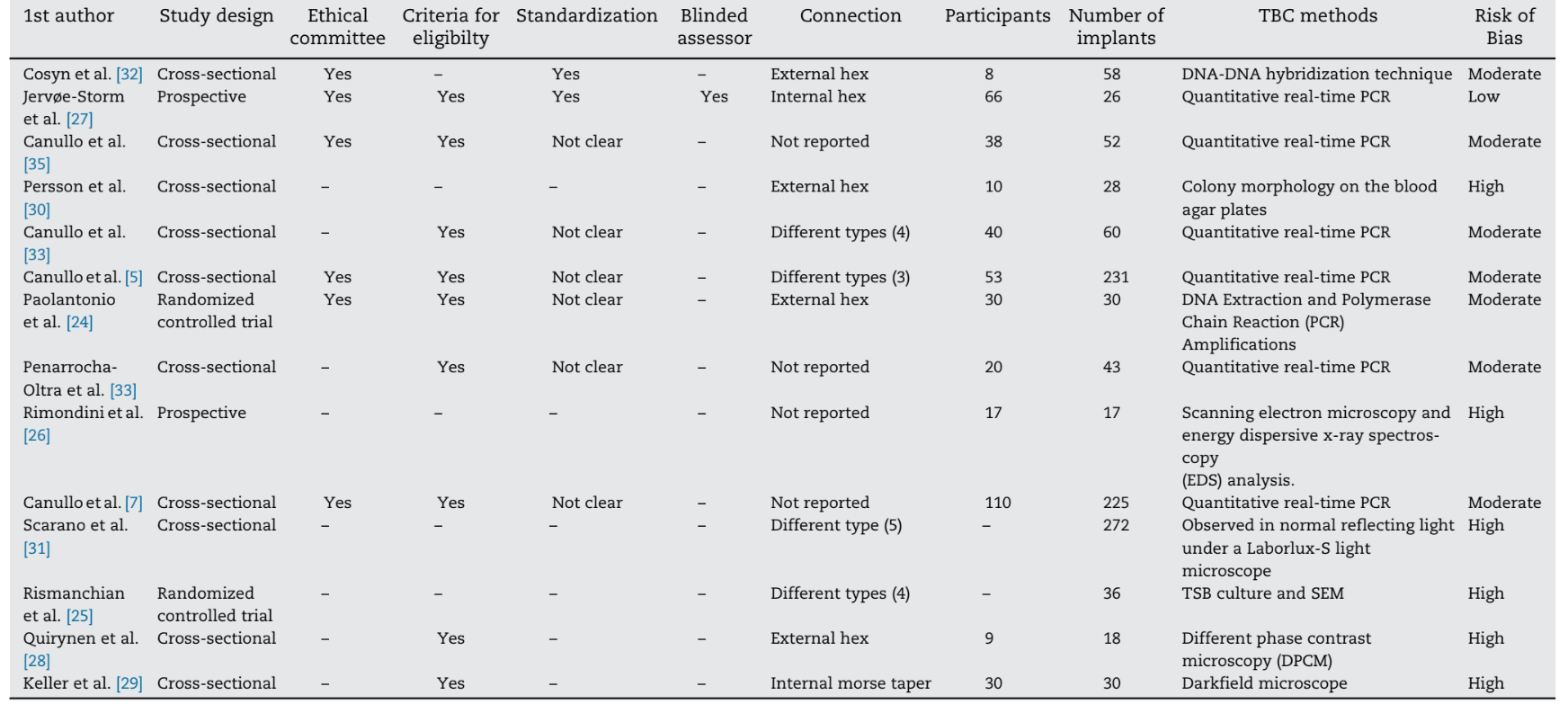
Учитывая адекватность соответствующих исследований, элементы были оценены, и был рассчитан процент положительно оцененных элементов. Оценка качества проводилась в два разных этапа, а именно на этапе I, где оценка качества основывалась на опубликованных статьях полного текста, выполненных независимо обоими рецензентами, и на этапе II, где разногласия разрешались в ходе обсуждения. После сбора оценок на этапе II оценки качества была завершена общая оценка вероятного риска предвзятости (низкий, умеренный или высокий) для каждого выбранного исследования. Низкий риск предвзятости оценивался, когда все критерии были выполнены, умеренный риск считался, когда один или несколько критериев были частично выполнены, и высокий риск предвзятости оценивался, когда один или несколько критериев не были выполнены (Руководство Кокрана по систематическим обзорам вмешательств, версия 5.1.0. http://www.cochrane.org/resources/handbook).
2.6. Меры и анализ результатов
Были проведены описательная статистика, мета-регрессия и мета-анализ на основе сопоставимых исследований, сообщающих об одних и тех же результатах. Микробиота, присутствующая в IAI имплантатов, функционирующих как минимум 1 год, была рассмотрена для анализа данных. BCs граммоотрицательных бактерий, связанных с хроническим пародонтитом (P. gingivalis, T. forsythia, T. denticola, P. intermedia и Fusobacterium nucleatum), были извлечены и определены как первенная переменная результата. Включенная микробиота для анализа регулярно обнаруживается на участках периимплантита и, как было установлено, увеличивает риск потери костной ткани вокруг импланта и прогрессирования заболевания. Средние различия были объединены с использованием моделей случайных эффектов. Гетерогенность между исследованиями, анализ подгрупп, мета-анализ и лесные графики были рассчитаны с использованием программного обеспечения (Comprehensive Meta-Analysis V3; Biostat, Englewood, NJ, USA).
Результаты
3.1. Выбор исследований
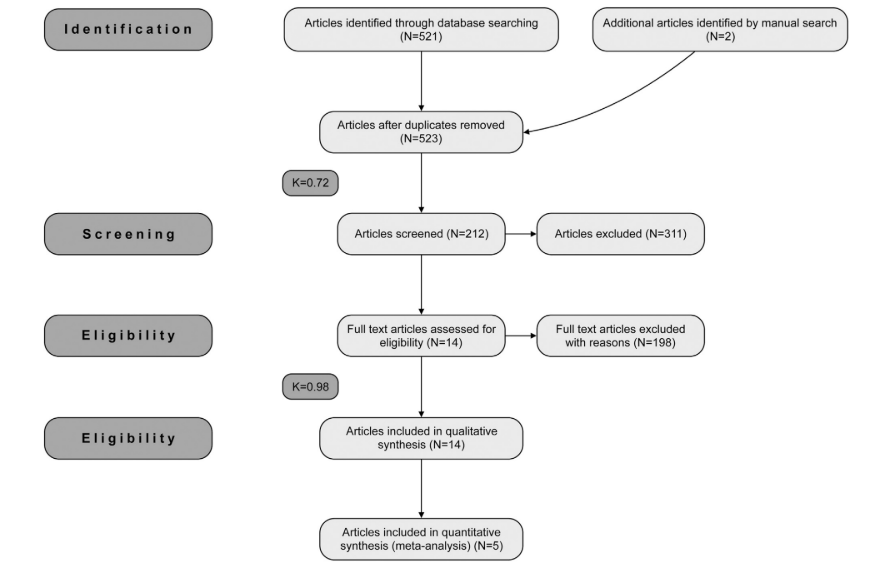
Всего было найдено 523 потенциально релевантных заголовка и аннотаций после электронного и ручного поиска. На первом этапе отбора 309 статей были исключены на основе заголовков и аннотаций (k=0.72). На втором этапе были оценены полные тексты оставшихся 212 публикаций, и 198 статей были исключены, так как они не соответствовали критериям включения (k=0.98). В итоге было отобрано 14 статей, в которых представлены данные по 1126 имплантатам, которые соответствовали критериям включения и оценке качества, необходимым для данного систематического обзора (Рис. 1).
3.2. Характеристики исследования
14 выбранных статей были опубликованы в период с 1993 по март 2015 года, из которых две были РКИ, две проспективные когортные исследования и десять поперечных исследований. Только одно проспективное клиническое исследование было написано в соответствии с заявлением STROBE для наблюдательных исследований (http://www.strobe-statement.org). Таким образом, прямое сравнение между выбранными статьями было невозможно.
3.3. Риск предвзятости в исследованиях
Ни одно из ретроспективных исследований не смогло выполнить все требования. Одна публикация была связана с низким риском предвзятости, семь — с умеренным риском предвзятости и шесть — с высоким риском предвзятости. Включенные статьи получили минимальную оценку при оценке подачи в этические комитеты (6/14), наличия слепых оценщиков (2/14), стандартизации процедур (1/14) и наличия критериев приемлемости (9/14) (Таблица 1).
3.4. Меры и мета-регрессионный анализ
3.4.1. Бактериальная утечка в IAI
Все выбранные исследования сообщили о контаминации IAI и поверхности абатмента у пациентов, получающих сборку двухступенчатой имплантационной системы. Количественная полимеразная цепная реакция в реальном времени (ПЦР) была проведена для BC в 7 из 14 исследований, где были проанализированы следующие патогены: Aggregatibacter actinomycetemcomitans, P. gingivalis, T. forsythia, T. denticola, P. intermedia, Parvimonas micra, F. nucleatum, C. rectus, Eikenella corrodens, Candida albicans, Enterococcus faecalis и Porphyromonas aeruginosa. В одном исследовании использовалась техника гибридизации ДНК-ДНК в шахматном порядке, в то время как в других шести исследованиях использовались различные техники, включая сканирующую электронную микроскопию для изучения морфологии колоний. В одном исследовании была описана прогрессивная колонизация периодонтальными патогенными бактериями внутренних частей двухкомпонентных имплантов. В другом исследовании внутрикоронковые компоненты фиксированных реставраций на винтовом креплении были сильно загрязнены во всех образцах. Контаминация винтов абатмента, вероятно, произошла из периимплантного сулкуса через IAI и интерфейс абатмент-протез. Аналогично, были обнаружены значительные различия в антибиотикорезистентных нозокомиальных бактериях (E. faecalis и P. aeruginosa) между внутренними и внешними компонентами импланта между здоровыми периимплантными сулкусами и имплантами, пораженными периимплантитом. Что касается отсутствия/наличия анализируемых бактерий, то значительных различий между анализом в периимплантном сулкусе и соединениями внутри поверхностей абатментов не было найдено. Микробный состав на соседних зубах напоминал состав, найденный в периимплантном сулкусе, с высокой частотой для P. gingivalis, T. forsythia, P. intermedia, P. micra и E. corrodens.
Два сравнительных исследования между здоровыми перимплантными условиями и имплантатами, пораженными периимплантитом, сообщили о бактериальном загрязнении в обеих группах. Виды оранжевого комплекса (P. intermedia, P. micra, F. nucleatum) были наиболее распространены на всех анализируемых участках для обеих групп. Внутри соединения имплантата преобладание анализируемых видов было более выраженным в группе с периимплантитом и варьировало от 1.1% A. actinomycetemcomitans до 98.9% F. nucleatum. Виды с ≥50% распространенности: P. gingivalis, T. denticola, P. intermedia, F. nucleatum, C. rectus, E. corrodens, T. forsythia и P. micra.
3.4.2. Бактериальная утечка в IAI в зависимости от конструкции соединения абатмента
Выбранная выборка показала большую гетерогенность в отношении типа IAI. Четыре исследования сообщили о внешних шестиугольных соединениях, а два исследования - о внутренних шестиугольниках или соединениях с конусом Морса. Четыре исследования использовали различные конструкции IAI, в то время как тип IAI не был указан в других 4 манускриптах.
Оценка четырех различных ИАИ показала, что все проанализированные соединения продемонстрировали загрязнение после 5 лет функциональной нагрузки. Также выяснилось, что дизайн соединения мог qualitatively и quantitatively повлиять на уровни BC, особенно внутри соединений имплантатов, показывая лучшие результаты для конусного соединения. Аналогично, различные типы абатментов показали значительное различие в среднем размере микрозазора в течение первых 5 часов нагрузки. Однако значительного влияния микропроникновения не было найдено через 24 часа, 48 часов и 14 дней на уровни BC. Тем не менее, использование стандартных абатментов значительно уменьшило размер микрозазора по сравнению с индивидуальными. Исследование пришло к выводу, что микропроникновение в области соединения было сопоставимо для всех проанализированных абатментов.
3.4.3. Мета-регрессия и анализ подгрупп
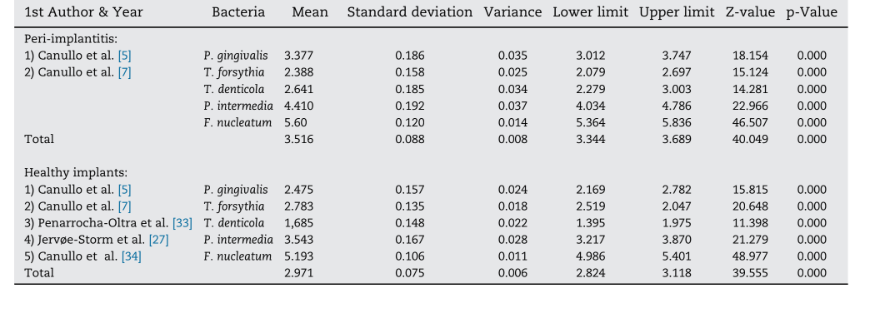
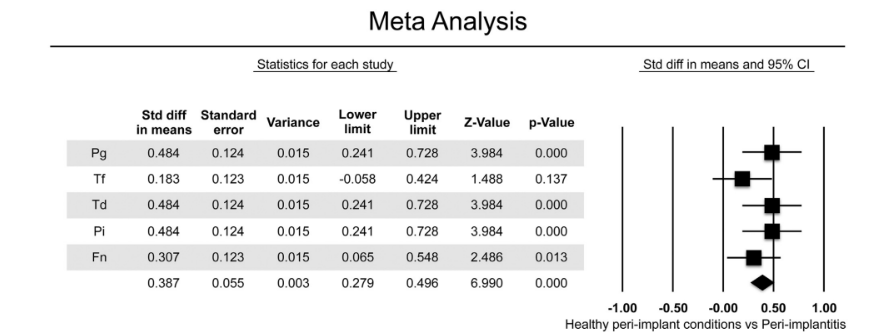
В мета-анализ было включено пять исследований, в которых в общей сложности было 622 импланта (n=223 с периимплантитом; n=399 с здоровыми периимплантными условиями), функционирующих не менее 1 года. BC грамм-отрицательных анаэробов показал связь с хроническим пародонтитом и был признан увеличивающим риск потери костной ткани вокруг имплантата и прогрессирования заболевания из-за присутствия пародонтальных патогенов (P. gingivalis, T. forsythia, T. denticola, P. intermedia, F. nucleatum) (Таблица 2)]. Мета-анализ учитывал бактерии, которые были оценены во всех выбранных исследованиях. Два из пяти исследований сравнили BC в здоровых периимплантных условиях и имплантах, пораженных периимплантитом. Мета-анализ показал более высокие средние значения для BC всех проанализированных грамм-отрицательных бактерий, за исключением T. forsythia в имплантах с периимплантитом (Рис. 2). В целом, средние различия в BC были статистически значительными между двумя проанализированными группами, с более высокими значениями в имплантах с периимплантитом (разница: 0.387 ± 0.055; 95% CI 0.279–0.496, p=0.000).
Обсуждение
Этот систематический обзор оценил микробную колонизацию на уровне имплантатов IAI и связал ее с возможным началом периимплантита. Имплантаты в один блок были исключены из анализа из-за супракрестального положения их IAJ: на самом деле, это местоположение, из-за аэробной среды, приводит к совершенно другой микробиологической композиции.
В данном обзоре, за исключением T. forsythia, значительно более высокая BC была выявлена у имплантатов, пораженных периимплантитом, по сравнению со здоровыми периимплантными карманами для всех граммотрицательных вероятных пародонтопатогенов. Для T. forsythia была обнаружена только тенденция к более высокой BC.
Включенные исследования оценивали микробиоту на уровне IAI у пациентов, которые получили двухступенчатые системы имплантатов с различными конструкциями соединения имплантата и абатмента. Тем не менее, два исследования сообщили о загрязнении IAI независимо от конструкции соединения. Невозможно было провести различие между восстановлением на винтовом и цементном удержании, предполагая, что соединение коронки и абатмента расположено более коронально, и что зазор заполнен цементом. Более того, включенные рукописи не нашли различий между погруженными и непогруженными имплантатами в микробной колонизации.
Наличие бактериального загрязнения на уровне ИАИ, размещенного на уровне альвеолярной кости, было продемонстрировано как связанное с значительным инфильтрацией воспалительных клеток и потерей кости. Увеличение накопления острых воспалительных клеток рядом с ИАИ указывает на сохранение химотактических стимулов из этого региона, поддерживающих непрерывный набор нейтрофильных гранулоцитов. Кроме того, наличие воспалительного инфильтрата периимплантной ткани на интерфейсахFixture-abutment также было вызвано микробным внутренним загрязнением.
Ряд исследований сообщал о том, что микробное загрязнение может происходить на уровне ИАИ как в имплантатах с здоровыми, так и с больными тканевыми условиями. Несмотря на то, что не было клинических признаков периимплантита, наличие бактериальных видов, связанных с этим состоянием, было явно повышено. Когда клинические и микробиологические характеристики у субъектов и имплантатов с здоровыми тканевыми условиями или периимплантитом были оценены, и данные из здоровых и больных имплантатов были сопоставлены в рамках одного субъекта (534 пациента; 1507 зубных имплантатов), были замечены четкие тенденции. Микробиологический анализ, полученный из трех мест (периимплантный сулкус (ПИС), внутренние части соединений имплантатов (ПИ), десневой сулкус соседних зубов) вместе с клиническими параметрами (кровотечение при зондировании, глубина зондирования кармана, индекс налета), наличие периимплантита было очевидно у 10,3% пациентов и у 7,3% имплантатов. Микробиологический анализ среди 53 пациентов, страдающих от периимплантита, не выявил значительных различий между анализом на ПИС и ПИ.
Микрогап на уровне IAI также может привести к механическим и биологическим осложнениям, включая переломы винтов абатмента и заболевания периимплантной ткани. Размер микрогапа и микробное утечка в разные моменты времени на IAI 4 различных абатментов к имплантатам Straumann оказали значительное влияние на средний размер микрогапа (p<0.001) и на среднее количество бактериальных колоний (CFU/mL), утечка которых происходила из IAI в течение первых 5 часов эксперимента (p=0.012). Однако микропроницаемость через 24 часа, 48 часов и 14 дней больше не имела значительного влияния (p=0.145).
Клинические и микробные различия между здоровыми периимплантными условиями и периимплантитом показали, что микробная распространенность была выше в группе периимплантита в трех местах, и различия в распространенности между различными типами бактерий были более выражены внутри соединения, чем в PIS (57 пациентов; 122 импланта).
Когда оппортунистические патогены (E. faecalis, P. aeruginosa) были выявлены в присутствии периимплантного заболевания на уровне PIS каждого импланта, в десневом кармане соседних зубов и в соединении и абатменте во внутренней части каждого импланта, были обнаружены значительные различия в наличии и количестве нозокомиальных бактерий вокруг больных имплантов. Это может свидетельствовать о важности дезинфекции соединения в случае лечения периимплантита.
Были предложены различные попытки снизить бактериальную колонизацию в области IAI в случае здоровых имплантатов. Однако применение 0,2% раствора хлоргексидина при двухэтапных операциях считается более распространенной практикой. Тем не менее, существуют противоречивые мнения о эффективности раствора хлоргексидина в предотвращении микробной колонизации в области IAI. Бактериальные эндотоксины обычно проникают в IAJ, но 0,2% раствор хлоргексидина не смог значительно устранить проникновение, по крайней мере, в долгосрочной перспективе. С другой стороны, в литературе не было предоставлено никаких указаний в случае имплантатов, пораженных периимплантитом.
Не только микробное утечка через зазор между супраструктурой и абатментом, но и конструкции имплантатов и материалы могут повлиять на потенциальный риск укрытия оральных микроорганизмов. Обычно соединения с конусом Морса развивают меньше бактерий по сравнению с четырехканальным конусным внутренним соединением. Аналогично, соединения с конусом Морса продемонстрировали благоприятные результаты в этом отношении по сравнению с трилобным цементированным соединением. С другой стороны, бактериальная микробиота, присутствующая внутри соединения имплантата и в PIS жидкости имплантатов с здоровыми периимплантными условиями с четырьмя различными системами имплантатов после как минимум 5 лет функциональной нагрузки, продемонстрировала микробиологическое загрязнение во всех типах соединений независимо от места (периимплантный сулкус, внутренняя часть соединения, поверхность абатмента и десневой сулкус соседних зубов).
С клинической точки зрения, текущие данные могут свидетельствовать о необходимости удаления комплекса коронки/абатмента и дезинфекции/стерилизации соединительных элементов как на стороне имплантата, так и на стороне абатмента в случае периплантита, в качестве дополнения к режимам поддержания стоматологических имплантатов.
Заключения
Этот мета-анализ показал, что бактерии могут легко колонизироваться на интерфейсе имплант-абатмент. С клинической точки зрения очевидно, что внутренние части IAI всегда следует считать загрязненными, даже в клинически здоровых условиях.
Марко Талларико, Луиджи Канулло, Мартина Канева, Мутлу Озкан
Ссылки
- Херманн Дж.С., Бусер Д., Шенк Р.К., Скулфилд Дж.Д., Кокран Д.Л. Биологическая ширина вокруг одно- и двухкомпонентных титановыми имплантами. Clin Oral Implants Res 2001;12:559–71.
- Цуге Т., Хагивара Й., Мацумира Х. Пограничная подгонка и микрощели интерфейса имплант-абатмент с внутренней антиротационной конфигурацией. Dent Mater J 2008;27:29–34.
- Шварц Ф., Хегевальд А., Беккер Дж. Влияние соединения имплант-абатмент и позиционирования обработанного воротника/микрощели на изменения уровня кристального кости: систематический обзор. Clin Oral Implants Res 2014;25:417–25.
- Венг Д., Нагада М.Ж., Белл М., Боско А.Ф., де Мело Л.Г.Н., Рихтер Е.Й. Влияние расположения и конфигурации микрощели на морфологию периплантной кости в погруженных имплантатах. Экспериментальное исследование на собаках. Clin Oral Implants Res 2008;19:1141–7.
- Канулло Л., Пенарроча-Ольтра Д., Ковани У., Боттичелли Д., Серино Г., Пеньярроча М. Клинические и микробиологические данные у пациентов с периплантитом: поперечное исследование. Clin Oral Implants Res 2015;27:376–82.
- Канулло Л., Пеньярроча Д., Клементини М., Яннелло Г., Микарелли Ч. Влияние обработки плазмой аргона на абатменты имплантатов у пациентов с историей пародонтальной болезни и тонким биотипом: радиографические результаты через 24 месяца наблюдения в рамках РКИ. Clin Oral Implants Res 2015;26:8–14.
- Канулло Л., Пеньярроча Д., Ковани У., Россетти П.Х.О. Микробиологические и клинические данные имплантатов в здоровом состоянии и с периплантитом. J Oral Maxillofac Implants 2015;30:834–42.
- Квиринен М., Боллен К.М., Эйсен Х., ван Стенберге Д. Микробное проникновение вдоль компонентов имплантатов системы Бранемарка. Исследование in vitro. Clin Oral Implants Res 1994;5:239–44.
- Пассос С.П., Гресслер Мэй Л., Фария Р., Озкан М., Боттино М.А. Промежуток между имплантатом и абатментом против микробной колонизации: клиническое значение на основе литературного обзора. J Biomed Mater Res B Appl Biomater 2013;101:1321–8.
- Каллан Д.П., Кобб К.М., Уильямс К.Б. Идентификация бактерий, колонизирующих внутренние поверхности интерфейса имплант-абатмент с помощью ДНК-проб: предварительное исследование. J Periodontol 2005;76:115–20.
- Херманн Дж.С., Скулфилд Дж.Д., Шенк Р.К., Бусер Д., Кокран Д.Л. Влияние размера микрощели на изменения кристальной кости вокруг титановыми имплантами. Гистометрическая оценка разгруженных несубмергированных имплантатов в собачьей челюсти. J Periodontol 2001;72:1372–83.
- Пиаттели А., Скаранно А., Паолантонио М., Ассенза Б., Легисса Г.К., Ди Бонавентура Г. Жидкости и микробное проникновение во внутреннюю часть соединений имплант-абатмент с цементным удержанием и с винтовым удержанием. J Periodontol 2001;72:1146–50.
- Пérez-Chaparro П.Ж., Дуарте П.М., Шибли Я.А., Монтенегро С., Ласерда Хелуй С., Фигейредо Л.С., и др. Текущий вес доказательств микробиологического профиля, связанного с периплантитом: систематический обзор. J Periodontol 2016;87:1295–304.
- Монье А., Суарес Ф., Галиндо-Морено П., Гарсия-Ногалес А., Фу Дж.Х., Ванг Х.Л. Систематический обзор потери кости вокруг коротких стоматологических имплантатов (<10 мм) для фиксированных протезов на имплантатах. Clin Oral Implants Res 2014;25:1119–24.
- Мохер Д., Либерати А., Тетцлафф Дж., Алтман Д.Г., Группа PRISMA. Методы систематических обзоров и мета-анализов, предпочтительные элементы отчетности для систематических обзоров и мета-анализов: заявление PRISMA. J Clin Epidemiol 2009;62:1006–12.
- Линдхе Дж., Мейле Дж., Группа D Европейского семинара по пародонтологии. Периплантные заболевания: консенсусный отчет шестого европейского семинара по пародонтологии. J Clin Periodontol 2008;35:282–5.
- Ланг Н.П., Берглунд Т., Рабочая группа 4 Седьмого Европейского семинара по пародонтологии. Периплантные заболевания: где мы сейчас? Консенсус Седьмого Европейского семинара по пародонтологии. J Clin Periodontol 2001;38:178–81.
- Миллер С.А., Форрест Дж.У. Улучшение вашей практики через принятие решений на основе доказательств: PICO, научитесь задавать хорошие вопросы. J Evid Based Dent Pract 2001;1:136–41.
- Грациани Ф., Фигеро Э., Эррера Д. Систематический обзор качества отчетности, измерений результатов и методов изучения эффективности профилактических и терапевтических подходов к периплантным заболеваниям. J Clin Periodontol 2012;39:224–44.
- Пьетурссон Б.Е., Цвахлен М., Ланг Н.П. Качество отчетности клинических исследований для оценки и сравнения эффективности восстановлений на имплантатах. J Clin Periodontol 2012;39:139–59.
- Момбелли А., Декалье Ф. Характеристики биопленок при периплантных заболеваниях. J Clin Periodontol 2011;38:203–13.
- Момбелли А. Микробиология и антимикробная терапия периплантита. Periodontol 2000 2002;28:177–89.
- Леонгардт Å, Дален Г., Ренверт С. Пятилетний клинический, микробиологический и радиологический результат после лечения периплантита у человека. J Periodontol 2003;74:1415–22.
- Паолантонио М., Перинетти Г., Д’Эрколе С., Грациани Ф., Катамо Г., Саммартино Г. Внутренняя деконтаминация стоматологических имплантатов: рандомизированное микробиологическое исследование в vivo на эффектах геля хлоргексидина. J Periodontol 2008;79:1419–25.
- Рисманчиан М., Хатами М., Бадриан Х., Халигиниджад Н., Гороохи Х. Оценка размера микрощели и микробного утечки в области соединения 4 абатментов с имплантатом Straumann (ITI). J Oral Implantol 2012;38:677–85.
- Римондини Л., Марин Ч., Брунелла Ф., Фини М. Внутренняя контаминация системы имплантатов из 2 компонентов после окклюзионной нагрузки и временной лутовки с устройством или без него. J Periodontol 2001;72:1652–7.
- Йервое-Шторм П.М., Епсен С., Йохрен П., Мерицке-Штерн Р., Энклинг Н. Внутренняя бактериальная колонизация имплантатов: связь с потерей кости вокруг имплантатов. Clin Oral Implants Res 2015;26:957–63.
- Квиринен М., ван Стенберге Д. Бактериальная колонизация внутренней части двухступенчатых имплантатов: исследование in vivo. Clin Oral Implants Res 1993;4:158–61.
- Келлер В., Браггер У., Момбелли А. Периплантная микрофлора имплантатов с цементными и винтовыми удерживаемыми супраструктурами. Clin Oral Implants Res 1998;9:209–17.
- Перссон Л.Г., Лекхольм У., Леонгардт А., Дален Г., Линдхе Дж. Бактериальная колонизация на внутренних поверхностях компонентов имплантатов системы Бранемарка. Clin Oral Implants 1996;7:90–5.
- Скаранно А., Ассенза Б., Пиаттели М., Иеззи Г., Легисса Г.К., Куаранта А. 16-летнее исследование микрощели между 272 человеческими титановыми имплантатами и их абатментами. J Oral Implantol 2005;31:269–75.
- Косин Дж., Ван Аелст Л., Коллаерт Б., Перссон Г.Р., Де Брюн Х. Периимплантный сулкус по сравнению с внутренними компонентами имплантата и супраструктуры: микробиологический анализ. Clin Implant Dent Relat Res 2009;13:286–95.
- Пенарроча-Ольтра Д., Россетти П.Х.О., Ковани У., Галлуччо Ф., Канулло Л. Микроутечка соединения имплант/абатмент из-за маневров по установке имплантата: поперечный микробиологический анализ имплантатов после 5 лет нагрузки. J Oral Implantol 2014;41:e292–6.
- Канулло Л., Пенарроча-Ольтра Д., Солдини Ч., Маццокко Ф., Пенарроча М., Ковани У. Микробиологическая оценка интерфейса имплант-абатмент при различных соединениях: поперечное исследование после 5 лет функциональной нагрузки. Clin Oral Implants res 2014;26:426–34.
- Канулло Л., Россетти П.Х.О., Пеньярроча Д. Идентификация Enterococcus faecalis и Pseudomonas aeruginosa на и в имплантатах у лиц с периплантным заболеванием: поперечное исследование. Int J Oral Maxillofac Implants 2015;30:583–7.
- Сокрански С.С., Хаффаджи А.Д., Хименес-Фиви Л.А., Ферес М., Магер Д. Экологические соображения в лечении инфекций пародонта, вызванных Actinobacillus actinomycetemcomitans и Porphyromonas gingivalis. Periodontol 2000 1999;20:341–62.
- Сокрански С.С., Хаффаджи А.Д., Смит С., Дафф Г.W. Микробиологические параметры, связанные с полиморфизмами гена IL-1 у пациентов с пародонтитом. J Clin Periodontol 2000;27:810–8.
- Броггини Н., МакМанус Л.М., Херманн Дж.С., Медина Р., Шенк Р.К., Бусер Д. Воспаление вокруг имплантата, определяемое интерфейсом имплант-абатмент. J Dent Res 2006;85:473–8.
- Броггини Н., МакМанус Л.М., Херманн Дж.С., Медина Р.У., Оутс Т.В., Шенк Р.К. Устойчивое острое воспаление на интерфейсе имплант-абатмент. J Dent Res 2003;82:232–7.
- Косин Дж., Эгбали А., Де Брюн Х., Коллис К., Клеймает Р., Де Рук Т. Немедленные одноимплантатные имплантаты в передней челюсти: 3-летние результаты серии случаев по реакции жестких и мягких тканей и эстетике. J Clin Periodontol 2011;38:746–53.
- Тесмер М., Уоллетт С., Кутузис Т., Лундгрен Т. Бактериальная колонизация интерфейса фиксатора-абатмента стоматологического имплантата: исследование in vitro. J Periodontol 2009;80:1991–7.
- Насименто К.Д., Пита М.С., Фернандес Ф.Х.Н.К., Педраззи В., де Албукерке Джуниор Р.Ф., Рибейро Р.Ф. Бактериальное прилипание на поверхностях абатментов из титана и циркония. Clin Oral Implants Res 2014;25:337–43.
- Кутузис Т., Уоллетт С., Кальдерон Н., Лундгрен Т. Бактериальная колонизация интерфейса имплант-абатмент с использованием динамической модели нагрузки in vitro. J Periodontol 2011;82:613–8.
- Ассенза Б., Триподи Д., Скаранно А., Перротти В., Пиаттели А., Леззи Г. Бактериальная утечка в имплантатах с различными соединениями имплант-абатмент: исследование in vitro. J Periodontol 2012;83:491–7.
- Паолантонио М., Перинетти Г., Д’Эрколе С., Грациани Ф., Катамо Г., Саммартино Г., и др. Внутренняя деконтаминация стоматологических имплантатов: рандомизированное микробиологическое исследование в vivo на эффектах геля хлоргексидина. J Periodontol 2008;79:1419–25.
- Романо Г.Е., Билтуцци М.Т., Кокарас А., Пастер Б.Ж. Бактериальный состав на соединении имплант-абатмент под нагрузкой in vivo. Clin Implant Dent Relat Res 2016;18:138–45.
