Каркасы на основе поли(ε-капролактон)а и диакрилата полиэтиленгликоля для биоинженерных имплантатов диска ВНЧС
Машинный перевод
Оригинальная статья написана на языке EN (ссылка для ознакомления) .
Аннотация
Темпоромандибулярный сустав (ТМС), соединение между мыщелком нижней челюсти и височной костью, разделен на два отдела (верхний и нижний) фибро-хрящевым диском. Диск ТМС состоит из аваскулярной и неиннервированной ткани с вискоэластичным поведением. Механически диск ТМС испытывает растягивающие, сжимающие и сдвиговые силы. Смещение или дегенерация диска ТМС могут привести к серьезным внутрисуставным расстройствам темпоромандибулярного сустава (РТМС). Несмотря на большое количество современных терапий/лечений, существует ограниченное количество вариантов лечения тяжелых внутрисуставных РТМС. Стратегией решения этой проблемы может стать использование интерпозицийного материала для замены поврежденного диска ТМС, который будет постепенно разлагаться и способствовать образованию новой ткани. В данной работе были использованы и протестированы три варианта: один с использованием термопластичного материала, поли(ε-капролактон) (PCL), другой с использованием фотополимеризуемого гидрогеля, полиэтиленгликоля диакрилата (PEGDA), и третий с использованием комбинации двух материалов. Полученные результаты продемонстрировали, что комбинация различных материалов может представлять собой значительное преимущество в тканевой инженерии диска ТМС и в тканевой инженерии хряща в целом.
Введение
Темпоромандибулярный сустав (ТМС) является двусторонним соединением между мыщелковым отростком нижней челюсти и ямкой нижней челюсти и суставным бугорком височной кости. Между костными структурами располагается фиброхрящевой диск, который прикреплен к фиброзной капсуле по краям и делит сустав на две полости: верхнюю и нижнюю.
Диск ТМС состоит из аваскулярной, неиннервированной фиброхрящевой ткани с вискоэластичным поведением. Диск имеет эллиптическую форму, длина в медиолатеральном направлении больше, чем в антеропостериорном (19 и 13 мм соответственно у человека). Анатомически диск ТМС можно разделить на три области: передняя полоса, промежуточная зона и задняя полоса. Промежуточная зона значительно тоньше полос (≈1 мм у человека), а задняя полоса является самой толстой областью диска (≈4 мм у человека). Основная часть диска ТМС состоит из воды (≈73 %). Кроме воды, диск ТМС состоит из клеток (фибробластов, фиброцитов и клеток, похожих на хондроциты, с округлой формой) и внеклеточного матрикса (ВКМ) из плотных коллагеновых волокон (≈80 % по сухому весу), эластичных волокон (≈2 %) и гликозаминогликанов.
Эта бикавитарная форма соответствует анатомии кости сустава и является необходимой для функций ВНЧС. Как и в других суставах, диск ВНЧС уменьшает трение в суставе и распределяет нагрузку внутри сустава. Более того, он помогает выравниванию и стабилизации сустава во время вращения и трансляции благодаря некоторой гибкости, обеспечиваемой промежуточной областью. Диск ВНЧС имеет вискоэластичное поведение и испытывает растягивающие, сжимающие и сдвиговые силы. Сообщенные сжимающие свойства диска ВНЧС крайне непоследовательны, варьируясь от десятков до десятков тысяч кПа. Что касается различных областей, передние и задние полосы, похоже, имеют более высокие сжимающие свойства, чем промежуточная зона.
Дегенерация и смещение диска ВНЧС могут привести к расстройствам ВНЧС (РВНЧС). По оценкам, 25% населения могут испытывать симптомы РВНЧС, такие как: боль в суставе и окружающих мышцах; щелчки; дискомфорт при движении челюсти; скрежет зубами. Большинство РВНЧС успешно лечатся неинвазивными методами (например: физиотерапия, окклюзионные шины/корректировки и фармакология), но в некоторых случаях необходимо прибегнуть к хирургии (например: артроцентез, артроскопия, дископексия, дисцектомия и полная замена сустава).
Анатомия, эквивалентная человеческому ВНЧС, была изучена у различных животных. Некоторые из самых распространенных моделей включают свиней, овец, коз, коров, собак, крыс и кроликов. В этой работе геометрия имплантатов диска ВНЧС была получена с помощью обратного проектирования диска ВНЧС черной мериносовой овцы (Ovies aries).
В последние два десятилетия область Tissue Engineering (TE) диска ВНЧС растет как многообещающее решение для ТМД, нацеливаясь на восстановление и регенерацию диска. Были разработаны различные подходы, использующие или не использующие каркасы, разнообразные материалы и включение некоторых факторов роста.
Каркасы, используемые в TE диска ВНЧС, были произведены из полиамида, полигликолевой кислоты (PGA), поли(глицеролсебаката) (PGS), полимолочной кислоты (PLA), поли-L-молочной кислоты (PLLA), политетрафторэтилена (PTFE) и других натуральных биоматериалов, таких как коллагеновые гидрогели и из деклеточных дисков ВНЧС свиней. В последние годы, из-за их медленной скорости деградации, каркасы и пены из поли(ɛ-капролактон) (PCL) были широко исследованы, учитывая медленную скорость регенерации фибро-хряща.
Эта работа сосредоточена на разработке каркаса на основе PCL и PEGDA для биоинженерного имплантата диска ВНЧС, с характеристиками, близкими к естественной ткани, произведенного с использованием технологий быстрого прототипирования и осуществимого хирургического подхода.
Материалы и методы
Различные каркасы были произведены с использованием технологий обратного проектирования и аддитивного производства, с целью замены и содействия регенерации ECM диска ВНЧС. В этом исследовании было произведено три типа 3D-матриц: i) гидрогель PEGDA через фотополимеризацию, ii) каркасы PCL с использованием моделирования экструзией (FDM), iii) комбинация обоих.
Производство каркаса из поли(ɛ-капролактон)
Поли(ɛ-капролактон) (PCL) является биосовместимым и биоразлагаемым полиэстером (12-24 месяца), который, как показано, способен поддерживать широкий спектр типов клеток и является материалом, одобренным Управлением по контролю за продуктами и лекарствами США (FDA). Процесс экструзии или моделирование экструзией (FDM) состоит в экструзии (термо)пластика или воска, в данном случае PCL (в виде нити или гранул), через сопло, которое создает предполагаемый слой за слоем. Сопротивляющиеся нагреватели, покрывающие подающий канал и сопло, используются для поддержания материала чуть выше его температуры плавления (около 60ºC для PCL). Это позволяет материалу легко течь через сопло, связываясь с нижележащим слоем и достигая быстрой затвердевания.
В первом эксперименте было исследовано влияние температуры сопла на механическое поведение каркасов. Таким образом, каркасы PCL 6500 (Perstorp) (n=4) были произведены с использованием машины BioExtruder (CDRSP, Лейрия, Португалия) при температуре сопла 80ºC (группа T80) и 86ºC (группа T60). Кроме того, температуры депозита и системы каналов/разделителей составили соответственно 80ºC и 100ºC, использованное сопло имело диаметр 300 мкм, а скорости депонирования и поперечного перемещения составили 14,5 об/мин и 10 мм∙с-1 соответственно. Финальные каркасы PCL, геометрия которых была получена методом обратного проектирования диска ВНЧ овцы, имели основание 278 ± 2 мм2 и толщину среза 280 мкм.
Производство гидрогелей PEGDA
Поли(этиленгликоль), PEG, является биосовместимой, гидрофильной, нейтральной и высокомобильной полимерной цепью, которая использовалась в тканевой инженерии костей и хрящей, среди прочих биомедицинских приложений, таких как системы контролируемого высвобождения лекарств. Поли(этиленгликоль) диакрилат, PEGDA, является одним из производных PEG, который легко манипулируется в гидрогели с помощью фотополимеризации с использованием биосовместимых фотоинициаторов, таких как DMPA (2,2-Диметокси-2-фенил-ацетофенон), и воздействия ультрафиолетового света с длинной волной, вызывая сшивание.
Гидрогели PEGDA (Sigma-Aldrich) (n=4) были произведены с двумя различными концентрациями: 20% (группа H20) и 30%w/V (группа H30) с буфером 2-[4-(2-гидроксиэтил)пиперазин-1-ил]этансульфоновой кислоты (HEPES) (Sigma-Aldrich). Фотополимеризация была вызвана с использованием 0,1% w/V фотинициатора 2,2-диметокси-1,2-дифенилэтанона (DMPA, Sigma-Aldrich) при воздействии УФ-света (365 нм). Правильная форма диска ВНЧС была получена с помощью инструмента для резки, созданного исключительно для этой цели.
Обработка поверхности
Для улучшения гидрофильности каркасов PCL были выполнены две основные стратегии: i) 4 каркаса (из группы T86) были помещены в 1M раствор гидроксида натрия (NaOH) на примерно 24 часа (PNaOH); ii) другие 4 каркаса (из группы T80) были помещены в раствор PEGDA перед фотополимеризацией (PH).
Механические испытания
Механическое поведение каркасов и гидрогелей оценивалось с помощью одноосных неконфинированных испытаний на сжатие с использованием универсальной испытательной машины с использованием скорости растяжения 1 мм.мин-1. Перед механическими испытаниями площадь каждого каркаса была определена с использованием программного обеспечения ImageJ2. Сила, F (Н) и деформация (мм) записывались в любой момент времени в ходе испытаний, и значения сжимающего напряжения и деформации были определены для построения графиков напряжение-деформация. Таким образом, модуль упругости при сжатии был оценен в соответствии с наклоном начального линейного участка построенных кривых.
Статистический анализ
Одномерная описательная статистика (среднее значение и стандартное отклонение) механического поведения была определена для каждой группы. Значимые различия между группами оценивались с помощью однофакторного дисперсионного анализа (ANOVA). Пост-хок тесты (тест Тьюки) проводились для выявления значительных различий (p<0.05) для различных температур сопел во время производства и для поверхностной обработки, в каркасах, а также для различных концентраций PEGDA в случае гидрогелей. Эти тесты проводились с использованием GraphPad Prism 6 (GraphPad Software, Inc.) и Excel 2016 (Microsoft Corporation). ImageJ2 (общественное достояние) использовался для определения площадей каркасов и гидрогелей.
Результаты и обсуждение
С помощью Bioextruder мы смогли успешно произвести воспроизводимые каркасы (максимум 26 x 13 x 4 мм) с заданной геометрией, полученной с использованием обратного проектирования родного диска (Рис. 1).

Оценка влияния температуры сопла
Каркасные диски TMJ из PCL были успешно получены при использовании двух различных температур сопла. Результаты, полученные в ходе одноосного неограниченного испытания на сжатие, показывают, что между двумя группами существуют значительные различия (p<0.05) (см. рис. 3). Группы T80 и T86 продемонстрировали модуль сжатия 31.8 ± 1.5 МПа и 23.9 ± 1.8 МПа соответственно.
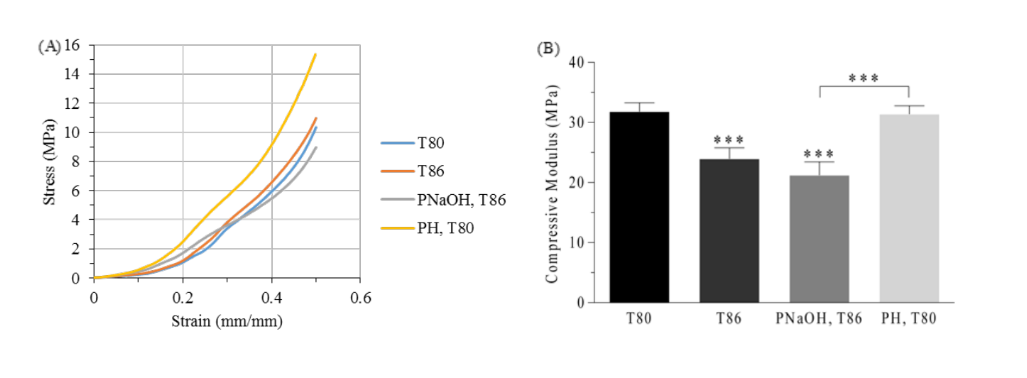
Согласно литературе, температура непосредственно влияет на ширину дороги, влияя на конечную пористость (более высокая температура приводит к более низкой пористости) структур и, следовательно, на их механическое поведение. Более низкая температура позволяет материалу быстрее затвердевать, уменьшая возможные изменения в геометрии каркасов. Эти изменения могут происходить при более высоких температурах производства, потому что материал, находясь в вязком состоянии, подвержен воздействию силы тяжести, и каркасы становятся слегка плоскими. Этот эксперимент соответствует ожидаемому результату.
Оценка влияния концентрации PEGDA на механические свойства гидрогелей
Как показано на рисунке 2, между двумя группами гидрогелей представлены значительные различия (p<0.05). Гидрогели, произведенные с концентрацией PEGDA 20% w/V, показали почти вдвое меньший модуль сжатия и треть предельной прочности (1.30 ± 0.15 МПа и 0.30 ± 0.03 МПа соответственно) по сравнению с гидрогелями, произведенными с 30% w/V PEGDA (2.21 ± 0.16 МПа и 1.01 ± 0.11 МПа). Несмотря на это, гидрогели группы H30 оказались очень хрупкими при изгибе или растяжении. Таким образом, для производства каркасов группы PH использовались гидрогели, аналогичные группе P20.
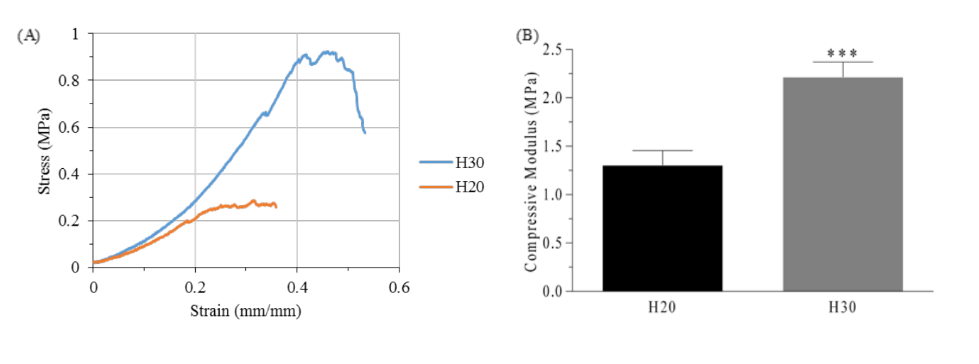
Влияние обработки поверхности
Обработка поверхности каркасов PCL не привела к значительным различиям в механическом поведении каркасов. Компрессионный модуль группы PNaOH (21.2 ± 2.2 МПа) немного снизился по сравнению с контрольной группой (T86), но эти различия не были значительными (p>0.05). Небольшое снижение механических свойств связано с деградацией поверхности, вызванной раствором NaOH - уменьшением диаметра волокон, который становится нерегулярным вдоль волокна. Таким образом, каркасы теряют массу, и их пористость увеличивается, что приводит к снижению механических свойств при сжатии.
С другой стороны, добавление гидрогеля в группу PH не вызвало значительных различий в компрессионных упругих модулях (31.4 ± 1.4 МПа) по сравнению с контрольной группой (T80). Кроме того, гидрогель, похоже, значительно увеличивает смазку и гибкость каркасов, и это может помочь в клеточной адгезии благодаря увеличению его гидрофильности.
Использование PCL в тканевой инженерии хрящей, в частности в фиброзно-хрящевой ткани диска ВНЧС, является недавним. Хотя первоначальная гидрофобность PCL, обработка поверхности NaOH может улучшить его гидрофильность и клеточную адгезию благодаря неровностям поверхности. Более того, внедрение гидрогеля PEGDA является авангардным подходом и может указать правильное направление для успешного биоинженерного имплантата диска ВНЧС. Сочетание двух различных биоматериалов (и связанных с ними технологий производства) может привести к значительным преимуществам в тканевой инженерии диска ВНЧС. В этом подходе PCL обеспечивает необходимую механическую прочность, а его медленная скорость деградации совместима с медленной скоростью роста фиброзно-хрящевой ткани, в то время как гидрогель PEGDA способствует клеточной адгезии, увеличивает смазку имплантата и позволяет интеграцию факторов роста. Хотя PCL обладает большей жесткостью, чем ткань диска ВНЧС, это может быть полезно в хирургии, так как позволяет легче установить имплантат, сокращая время и позволяя менее инвазивную операцию.
Заключение
Диск ВНЧС TE направлен на предложение альтернативы текущим методам лечения ТМД из-за дегенерации диска. Таким образом, комбинирование различных материалов возможно для производства биоинженерного имплантата, который лучше имитирует свойства родной ткани.
В этом исследовании мы успешно произвели каркас на основе PCL и PEGDA для биоинженерного дискового имплантата ВНЧС. Благодаря медленной скорости деградации PCL, этот материал совместим с медленной скоростью роста ткани диска ВНЧС. Более того, PCL обеспечивает важные механические свойства каркаса, и его относительная жесткость может представлять собой преимущество во время операции. С другой стороны, гидрогель PEGDA способствует клеточной адгезии и обеспечивает смазку. Таким образом, функции диска ВНЧС обеспечены: i) смазка позволяет уменьшить трение в суставе; ii) распределение внутрисуставной нагрузки обеспечивается геометрией каркаса и механическими свойствами материалов; ii) геометрия имплантата позволяет выравнивание и стабилизацию сустава.
В заключение, данная работа продемонстрировала, что сочетание различных материалов может представлять собой значительный прогресс в тканевой инженерии диска височно-нижнечелюстного сустава и в инженерии хрящей в целом.
Авторы: Луиш Франсиско, Карла Мора, Тânia Вiana, Давид Анджело, Педро Моруко, Нуну Алвеш
Ссылки:
- VanPutte, C., Regan, J., Russo, A., Seeley, R., Stephens, T. и Tate, P., Анатомия и физиология Сили, 10-е издание, Нью-Йорк, США, 2014
- Athanasiou, K. A., Almarza, A. A., Detamore, M. S. и Kalpakci, K. N., Тканевая инженерия хряща височно-нижнечелюстного сустава, 2009
- Stankovic, S., Vlajkovic, S., Boskovic, M., Radenkovic, G., Antic, V. и Jevremovic, D., Морфологические и биомеханические особенности диска височно-нижнечелюстного сустава: обзор недавних находок, Arch Oral Biol, 58 (2013) 1475-82
- Kalpakci, K. N., Willard, V. P., Wong, M. E. и Athanasiou, K. A., Сравнение диска височно-нижнечелюстного сустава между видами, J Dent Res, 90 (2011) 193-8
- Matuska, A. M., Muller, S., Dolwick, M. F. и McFetridge, P. S., Биомеханические и биохимические результаты деформации диска височно-нижнечелюстного сустава свиней, Arch Oral Biol, 64 (2016) 72-9
- Fazaeli, S., Ghazanfari, S., Everts, V., Smit, T. H. и Koolstra, J. H., Вклад коллагеновых волокон в механические сжимающие свойства диска височно-нижнечелюстного сустава, Osteoarthritis Cartilage, 24 (2016) 1292-301
- Kuo, J., Zhang, L., Bacro, T. и Yao, H., Зависимые от региона биполярные вязкоупругие свойства дисков височно-нижнечелюстного сустава человека при ограниченном сжатии, J Biomech, 43 (2010) 1316-21
- Tanaka, E. и Eijden, T. v., Биомеханическое поведение диска височно-нижнечелюстного сустава, Crit Rev Oral Biol Med, 14 (2003) 138-150
- Beek, M., Aarnts, M. P., Koolstra, J. H., Feilzer, A. J. и Eijden, T. M. G. J. v., Динамические свойства диска височно-нижнечелюстного сустава человека, J Dent Res, 80 (2001) 876-880
- Willard, V. P., Kalpakci, K. N., Reimer, A. J. и Athanasiou, K. A., Региональный вклад гликозаминогликанов в сжимающие свойства диска височно-нижнечелюстного сустава, J Biomech Eng, 134 (2012) 011011
- Ingawale, S. и Goswami, T., Височно-нижнечелюстной сустав: расстройства, лечение и биомеханика, Ann Biomed Eng, 37 (2009) 976-96
- Murphy, M. K., MacBarb, R. F., Wong, M. E., A., K. и Athanasiou, K. A., Расстройства височно-нижнечелюстного сустава: обзор этиологии, клинического управления и стратегий тканевой инженерии, Int J Oral Maxillofac Implants, 28 (2013) e393–e414
- Herring, S. W., Анатомия ВНЧС и животные модели, J Musculoskelet Neuronal Interact, 3 (2003) 391
- Bermejo, A., González, O. и González, J. M., Свинья как животная модель для экспериментов на височно-нижнечелюстном суставе, Oral Surc Oral Med Oral Pathol, 75 (1993) 18-23
- Angelo, D. F., Morouco, P., Alves, N., Viana, T., Santos, F., Gonzalez, R., Monje, F., Macias, D., Carrapico, B., Sousa, R., Cavaco-Goncalves, S., Salvado, F., Peleteiro, C. и Pinho, M., Выбор овец (Ovis aries) в качестве животной модели для исследований височно-нижнечелюстного сустава: морфологическая, гистологическая и биомеханическая характеристика диска сустава, Morphologie, 100 (2016) 223-233
- Mehrotra, D., Биоинженерия ВНЧС: обзор, J Oral Biol Craniofac Res, 3 (2013) 140-5
- Hunter, C. J., Инженерия фиброзного хряща, в: J. A. Burdick и R. L. Mauck (ред.), Биоматериалы для приложений тканевой инженерии: обзор прошлых и будущих тенденций, Springer, Нью-Йорк, 2011, стр. 363-389
- Allen, K. D. и Athanasiou, K. A., Выбор каркаса и факторов роста в инженерии диска височно-нижнечелюстного сустава, J Dent Res, 87 (2008) 180-185
- Juran, C. M., Dolwick, M. F. и McFetridge, P. S., Инженерная микропористость: повышение раннего регенеративного потенциала деклеточенных дисков височно-нижнечелюстного сустава, Tissue Eng Part A, 21 (2015) 829-39
- Springer, I. N. G., Fleiner, B., Jepsen, S. и Açil, Y., Культура клеток, полученных из хряща височно-нижнечелюстного сустава на нерассасывающемся каркасе, Biomaterials, 22 (2001) 2569–2577
- Hagandora, C. K., Gao, J., Wang, Y. и Almarza, A. J., Поли (глицерол себакат): новый материал каркаса для инженерии диска височно-нижнечелюстного сустава, Tissue Eng Part A, 19 (2013) 729-37
- Brown, B. N., Chung, W. L., Almarza, A. J., Pavlick, M. D., Reppas, S. N., Ochs, M. W., Russell, A. J. и Badylak, S. F., Индуктивный, основанный на каркасе, подход к регенеративной медицине для реконструкции диска височно-нижнечелюстного сустава, J Oral Maxillofac Surg, 70 (2012) 2656-68
- Kobayashi, E., Nakahara, T., Inoue, M., Shigeno, K., Tanaka, A. и Nakamura, T., Экспериментальное исследование in situ тканевой инженерии диска височно-нижнечелюстного сустава с использованием аутологичной костного мозга и коллагенового губчатого каркаса, Journal of Hard Tissue Biology, 24 (2015) 211 -218
- Olubamiji, A. D., Izadifar, Z., Si, J. L., Cooper, D. M., Eames, B. F. и Chen, D. X., Модулирование механического поведения 3D-печатных каркасов, имитирующих хрящ: влияние молекулярной массы и геометрии пор, Biofabrication, 8 (2016) 025020
- Legemate, K., Tarafder, S., Jun, Y. и Lee, C. H., Инженерия дисков ВНЧС человека с каркасами, выделяющими белки, напечатанными на 3D-принтере, J Dent Res, 95 (2016) 800-7
- Ratner, B. D., Hofffman, A. S., Schoen, F. J. и Lemons, J. E., Научная основа биоматериалов - Введение в материалы в медицине, Сан-Диего, Калифорния, 1996
- Ebnesajjad, S., Справочник по биополимерам и биодеградируемым пластиковым материалам - Свойства, переработка и применение, Великобритания, 2013
- Domingos, M., Chiellini, F., Gloria, A., Ambrosio, L., Bartolo, P. и Chiellini, E., Влияние параметров процесса на морфологические и механические свойства 3D биоэкструзированных каркасов поли(ε-капролактон), Rapid Prototyping Journal, 18 (2012) 56-67
- Sun, H., Mei, L., Song, C., Cui, X. и Wang, P., Внутреннее разрушение, абсорбция и выведение имплантата на основе PCL, Biomaterials, 27 (2006) 1735-40