Систематический обзор определения периимплантита: ограничения, связанные с различными предложенными диагнозами
Машинный перевод
Оригинальная статья написана на языке EN (ссылка для ознакомления) .
Аннотация
Цель: Целью данного комплексного систематического обзора было представить различные определения периимплантита, предложенные в литературе.
Материалы и методы: Электронные и ручные поиски литературы были проведены тремя независимыми рецензентами для выявления рукописей, сообщающих данные о определении периимплантита с клиническим диагнозом, написанных на английском языке и опубликованных до октября 2015 года. Были использованы несколько баз данных, включая PubMed, Embase, библиотеку Кокрана и базу серой литературы.
Результаты: Девяносто девять статей были признаны подходящими для обзора. Текущие данные предполагают использование однозначных определений случаев периимплантита, определяемых изменениями уровня кристаллической кости, наличием кровотечения при зондировании и/или гнойным выделением, с или без сопутствующего углубления периимплантных карманов. Однако для измерения этих изменений использовались несколько контрольных точек, включая различные уровни тяжести и годы наблюдения.
Заключение: Доступная научная литература предполагает отсутствие единого определения периимплантита. Будущие исследования, которые применяют последовательные определения случаев, должны быть рассмотрены.
Введение
Термин “периимплантит” был введен в начале 1960-х годов для описания инфекционных патологических состояний периимплантной ткани. Сегодня периимплантит является наиболее частым осложнением зубных имплантов и встречается с частотой от 1% до 47% на уровне импланта. В отличие от периимплантного мукозитиса (определяемого как наличие обратимого воспалительного инфильтрата мягких тканей, без дополнительной потери костной ткани за пределами первоначального физиологического ремоделирования кости), периимплантит характеризуется воспалительным процессом вокруг импланта, включая как воспаление мягких тканей, так и прогрессивную потерю поддерживающей кости за пределами физиологического ремоделирования костной ткани. Однако, как подчеркивается в недавних обзорах литературы и консенсусных конференциях, были сообщены различные определения периимплантита. Это может быть отчасти связано с отсутствием согласия по терминологии, этиологии, системам диагностики и прогноза.
Перимплантит описывается как заболевание с инфекционным компонентом, аналогичным хроническому периодонтиту. На 8-м Европейском семинаре по пародонтологии было согласовано, что следует принять определения, опубликованные в 200810 и 20118. Предложенное определение должно включать следующее: изменения уровня кристаллической кости, положительное кровотечение при зондировании (BOP) и/или гнойное выделение (SUP), с или без сопутствующих перимплантных карманов (глубина зондирования кармана, PPD). В настоящее время, хотя накопление налета по-прежнему считается основным этиологическим фактором, было показано, что существуют и другие потенциальные сопутствующие факторы риска заболевания, включая факторы пациента, хирургические и протезные факторы, которые, безусловно, могут способствовать его развитию.
В базе данных MeSH (Medical Subject Headings) термин «перимплантит» был введен в 2011 году и определен как воспалительный процесс с потерей поддерживающей кости в ткани, окружающей функционирующие зубные имплантаты. Несмотря на это очень четкое и полное определение заболевания, в клиническом применении терминологии возникают несоответствия и путаница. Все эти факторы вместе привели к различным интерпретациям и определениям этого общего возникающего заболевания. Кроме того, недавно гипотеза о неинфекционной реакции на инородное тело еще больше усложнила понимание этого вопроса. Целью настоящего систематического обзора было представить различные определения перимплантита, предложенные в литературе.
Материалы и методы
Настоящая статья была подготовлена в рамках выполнения консенсусного заявления, проведенного в Риме, Италия, в январе 2016 года. Этот систематический обзор был написан в соответствии с рекомендациями PRISMA (Предпочтительные элементы отчетности для систематических обзоров и мета-анализов) (http://www.prisma-statement.org/PRISMAStatement/PRISMA-Statement.aspx).
Сфокусированный вопрос был следующим: Существует ли единогласное определение периимплантита, включая клиническую диагностику. Исследовательский вопрос был адаптирован к формату PICO:
P = популяция: человеческие пациенты, полученные из клинических исследований, систематических обзоров, нарративных обзоров, консенсусных заявлений, комментариев или редакционных статей, у которых был хотя бы один функционирующий зубной имплант в течение минимум одного года, страдающие от периимплантита;
I = интервенция: клинические данные, собранные с целью установления тяжести перимплантита и определения новых критериев для классификации перимплантных заболеваний;
C = сравнение/контроль: клинические результаты перимплантита по сравнению с клиническими признаками пародонтита, а также с здоровыми пациентами;
O = результаты: клинические параметры и рентгенологическая оценка перимплантита: BOP, PPD, индекс кровоточивости, наличие SUP и потеря краевой кости (MBL).
Стратегия поиска
Первоначальная стратегия поиска, охватывающая английскую литературу с 1967 года до октября 2015 года, была выполнена онлайн для выявления соответствующих исследований, соответствующих критериям включения. Были проконсультированы следующие электронные базы данных: база данных PubMed Национальной библиотеки медицины США, Embase (Excerpta Medica dataBASE) и библиотека Кокрана. В соответствии с контрольным списком AMSTAR (Инструмент для оценки систематических обзоров) была проверена база данных серой литературы в отчете о серой литературе Нью-Йоркской академии медицины для поиска возможных неопубликованных работ. Скрининг проводился независимо и одновременно двумя экзаменаторами (MT и AM). Третий рецензент (LC) повторно оценил включенные и исключенные исследования. Поиск в электронных базах данных проводился с использованием комбинации булевых ключевых слов, включая MeSH и несколько терминов свободного текста (Таблица 1).
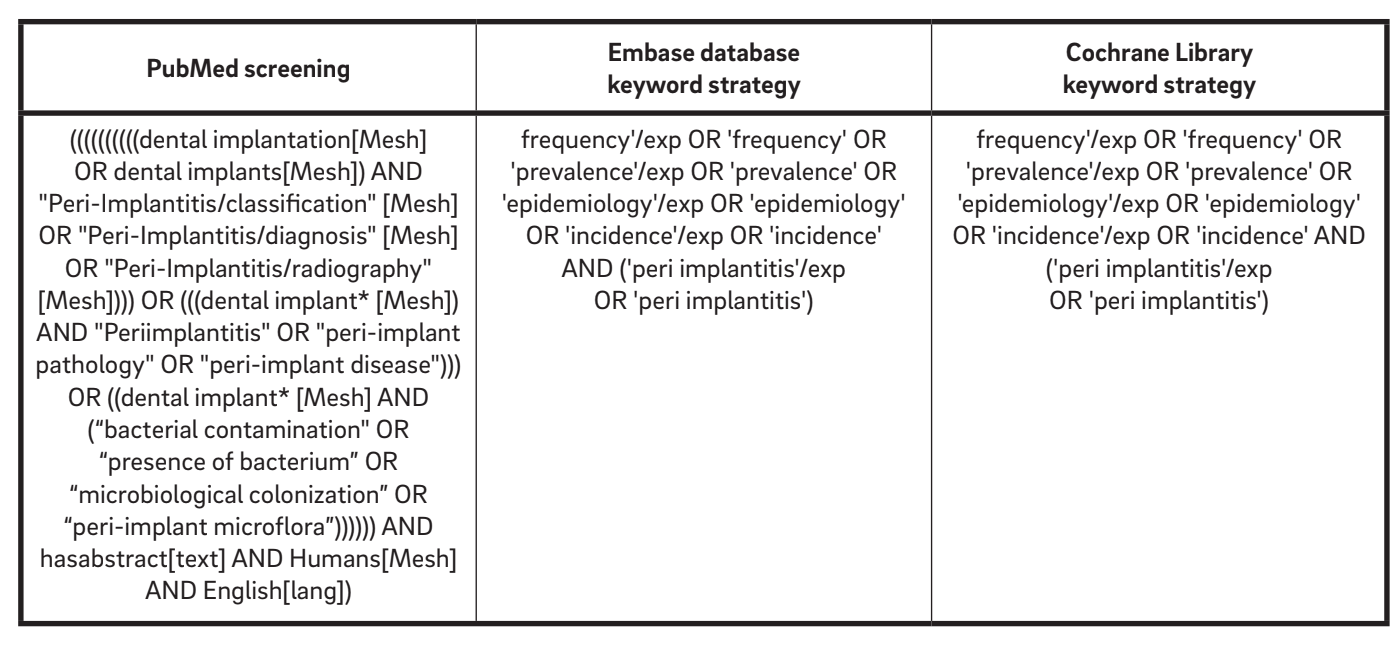
Критерии приемлемости
Для отбора статей были определены следующие критерии включения:
- написаны на английском языке;
- включают клиническое обследование человеческих пациентов;
- рандомизированные контролируемые клинические испытания имплантатов с ≥ 1 годом функционирования;
- перспективные и ретроспективные когортные исследования имплантатов с ≥ 1 годом функционирования;
- поперечные исследования с ≥ 1 годом функционирования; и
- систематические обзоры, нарративные обзоры, консенсусные заявления, комментарии или редакционные статьи.
Статьи были исключены, если они были
- исследованиями на животных;
- in vitro исследованиями;
- отчетами о локально или системно компрометированных участках и/или состояниях;
- отчетами с < 15 случаями;
- отчетами, касающимися мини-имплантатов, одноразовых имплантатов или лопастных имплантатов; или
- отчетами об имплантатах с < 1 годом функционирования.
Статьи без аннотаций, но с заголовками, связанными с целями данного обзора, были отобраны, чтобы полный текст можно было проверить на соответствие критериям включения. Полные тексты статей были получены для всех аннотаций и заголовков, которые, по-видимому, соответствовали критериям включения, и оценивались для включения теми же двумя экзаменаторами. Списки литературы выбранных исследований были проверены на наличие дополнительных статей, которые могли соответствовать критериям включения исследования. Кроме того, были проведены ручные поиски по спискам литературы выбранных систематических обзоров, ограниченные следующими журналами: Clinical Implant Dentistry and Related Research, Clinical Oral Implants Research, International Journal of Oral and Maxillofacial Implants, Journal of Clinical Periodontology и Journal of Periodontology. Любые разногласия между двумя рецензентами были разрешены после дополнительного обсуждения. Кроме того, согласие между исследователями было рассчитано на втором этапе. Финальный рецензент (LC) оценил возможные несоответствия между двумя рецензентами. Все полные тексты выбранных статей хранились в общих папках, доступных всем рецензентам.
Качественная оценка параметров для определения периимплантита
Была проведена описательная оценка для качественного анализа диапазона параметров, рассматриваемых для определения периимплантита как необратимого воспалительного состояния, приводящего к разрушению твердых тканей. Соответственно, были оценены следующие общие параметры: PPD, BOP, SUP и радиографический MBL. Такие параметры из различных статей были объединены для анализа вариации или однородности среди определений случаев периимплантита. Были созданы графики для представления вариации. В то время как PPD была классифицирована на три разные группы (< 3 мм, 3–5 мм и > 5 мм), радиографический MBL был категоризирован на четыре основные группы, в зависимости от основного эталона, принимая доставку протеза за базу: ≤ 1 мм, > 1–2 мм, > 3–4 мм и ≥ 5 мм.
Результаты
Процесс скрининга
Комбинации поисковых терминов и ручной поиск ссылок в выбранных статьях привели к списку из 1,061 заголовков. Из них 976 статей были исключены на основании оценки заголовка и аннотации, оставив 85 статей, подходящих для включения (k = 0.84). После применения критериев приемлемости всего 49 статей были рассмотрены. После выбора и чтения полных текстов статей была извлечена соответствующая информация из каждой статьи. Диаграмма стратегии поиска показана на Рисунке 1.
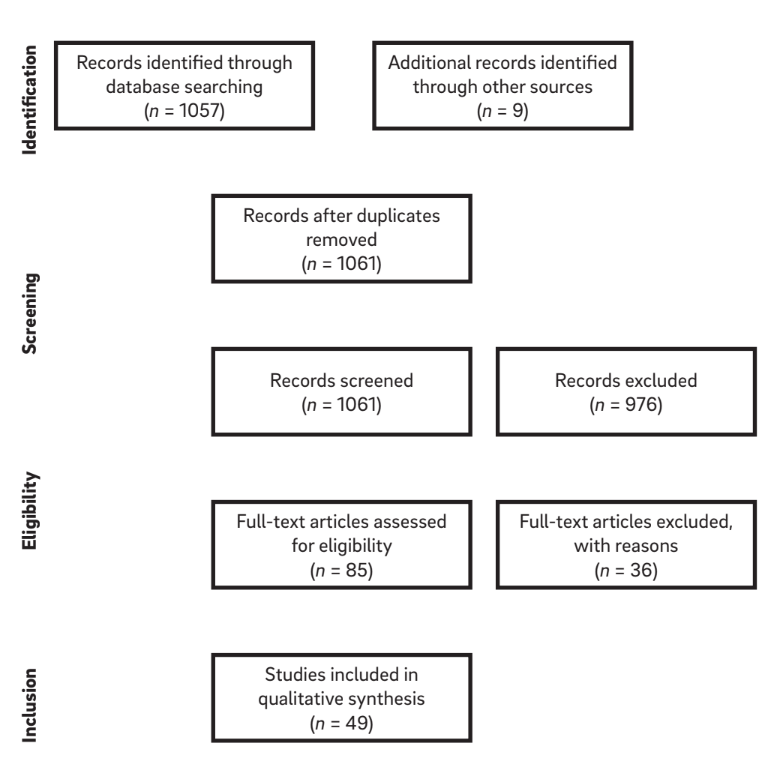
Определения “периимплантита”
Было выбрано восемнадцать рукописей, включая нарративные и систематические обзоры, консенсусные заявления и оригинальные статьи, и данные были извлечены. В 1965 году Левиньяк сообщил о воспалении мягких тканей вокруг имплантата с последующим разрушением кости и назвал это “периимплантитом.” В 1987 году Момбелли и др. описали периимплантит как инфекционное заболевание, которое имеет общие черты с хроническим пародонтитом. Тот же автор подчеркнул инфекционную природу этого патологического состояния, сосредоточив внимание на бактериальной нагрузке поверхности имплантата и последующем появлении воспалительной реакции мягких тканей рядом с зубными имплантатами, что иногда приводило к потере поддерживающей кости. Как и при пародонтите, было показано, что этиопатогенез периимплантита вызывается бактериальной инфекцией, которая активирует каскад цитокинов, приводя к воспалительной потере кости.
«Перимплантит» стал общепринятым термином в консенсусном отчете 1-го Европейского семинара по пародонтологии в 1993 году. Его описывают как необратимую воспалительную разрушительную реакцию вокруг функционирующих имплантатов, которая приводит к потере поддерживающей кости. 6-й Европейский семинар по пародонтологии представил модифицированное определение, которое не только признает, что перимплантит является поддающимся лечению состоянием, но и включает коллективный термин «перимплантное заболевание» как для перимплантного мукозита, так и для перимплантита.
С целью улучшения качества исследований по перимплантным заболеваниям 7-й Европейский семинар по пародонтологии рекомендовал использовать однозначные определения случаев: изменения уровня кристаллической кости и наличие BOP и/или SUP, с или без сопутствующего углубления перимплантных карманов. Наконец, Американская академия пародонтологии в 2013 году определила «перимплантит» как воспалительную реакцию, связанную с потерей поддерживающей кости за пределами первоначального биологического ремоделирования кости вокруг функционирующего имплантата.
Степень и тяжесть перимплантита редко сообщаются. Фрум и Розен предложили комбинацию BOP и/или SUP, PPD и степени радиографической MBL вокруг имплантата для классификации перимплантита на ранние, умеренные или продвинутые категории заболеваний. Аналогично, Деккер и др. предложили систему прогноза, основанную на диагнозе для каждой категории, следуя классификации прогноза Квока и Кэтона для естественного зубного ряда. В своем исследовании авторы заявили, что PPD, степень радиографической MBL, наличие SUP и подвижность имплантата были признаны наиболее критическими факторами для категоризации случаев как имеющих благоприятный, сомнительный, неблагоприятный или безнадежный прогноз.
Недавно Альбректссон и др. модифицировали концепцию перимплантита как потерю кости вокруг имплантата как клинически неблагоприятную, дисбалансированную реакцию на инородное тело, конкретно указывая, что остеоинтеграция — это процесс, при котором кость реагирует на зубной имплантат, образуя кальцифицированную структуру рядом с ним. Действительно, иногда эта реакция на инородное тело может привести к остеокластической активности, которая может разрушить поддерживающую кость. Авторы считают, что термин «перимплантит» вполне уместен, поскольку это не первичное заболевание, а осложнение клинически неблагоприятной, дисбалансированной реакции на инородное тело, которая является отправной точкой патологического процесса и последующих тканевых последствий.
В настоящее время, как предусмотрено консенсусом 7-го Европейского семинара по пародонтологии, предполагается, что инфекция всегда вызывается налетом и его продуктами; однако многочисленные факторы риска признаются специфически связанными с периимплантитом, такими как факторы, связанные с хирургией или протезированием, характеристики имплантата, курение и реакция организма.
Определение периимплантита с клинической и рентгенографической диагностикой
Было выбрано тридцать один манускрипт (Таблица 2) и извлечены данные. Информация о 1,711 пациентах с 5,432 имплантатами была проанализирована. Термин “периимплантит” обычно использовался для описания любого имплантата с различной степенью потери костной ткани, и четкое определение либо не было представлено, либо было извлечено непосредственно из терминологии.
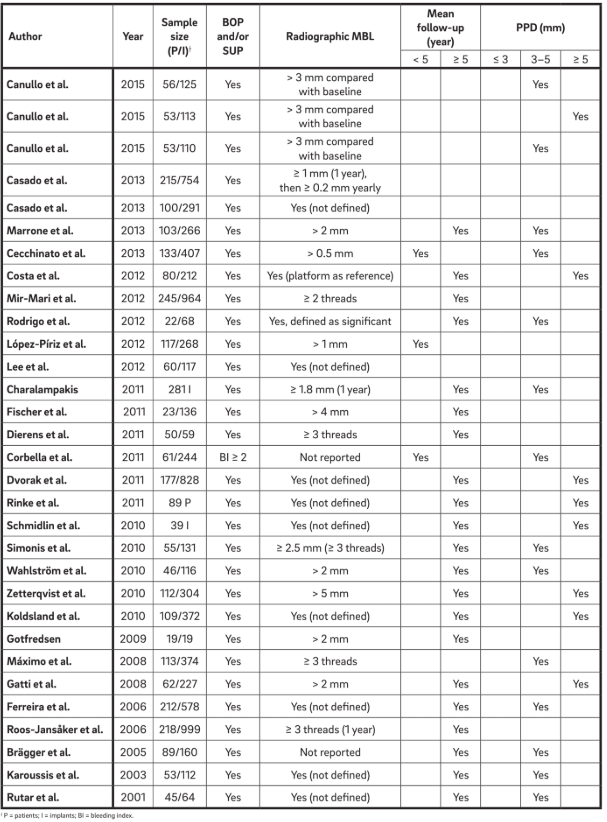
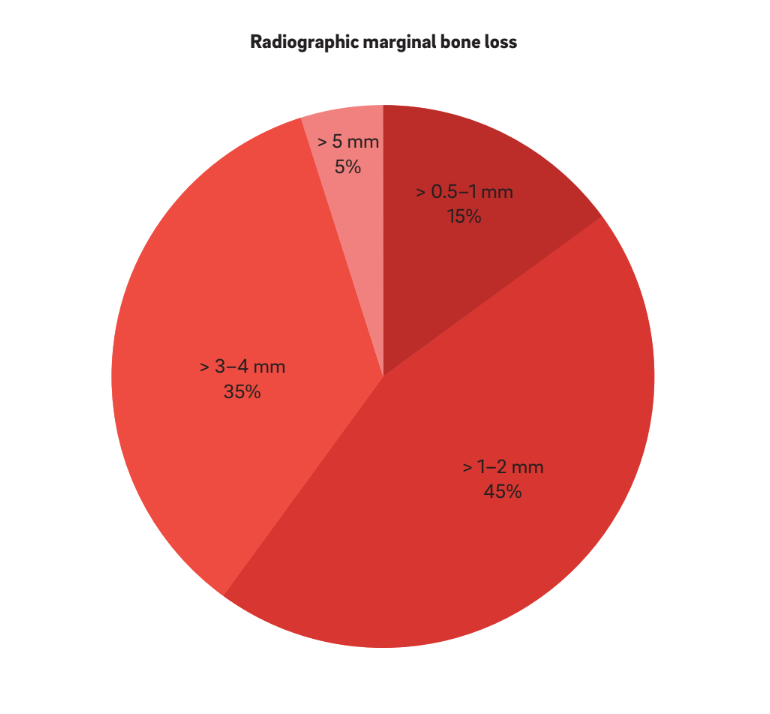
Четыре основные характеристики были использованы для определения "периимплантита". Интересно, что все авторы рассматривают BOP и SUP как индикаторы периимплантита. Этот подход учитывает исключительно периимплантит, вызванный налетом и инородными телами, когда воспалительная реакция часто вызывается биопленкой или ее продуктами и/или инородными веществами, такими как остаточный цемент. Более того, 22 исследования четко сообщили, что PPD является ключевым параметром для определения периимплантита. Ни одно исследование не считало PPD < 3 мм показателем периимплантита. Хотя подавляющее большинство (64%) исследований определило PPD = 3–5 мм как показатель периимплантита, оставшиеся 36% считали PPD > 5 мм эталоном (Рис. 2). Радиографический MBL ≥ 0.5–1 мм, > 1–2 мм, > 3–4 мм и ≥ 5 мм, принимая доставку протеза за базу, считался определяющим периимплантит в 15%, 45%, 35% и 5% исследований соответственно (Рис. 3). Таким образом, было высказано предположение, что радиографический MBL < 1 мм следует рассматривать как физиологическую ремоделирование кости.
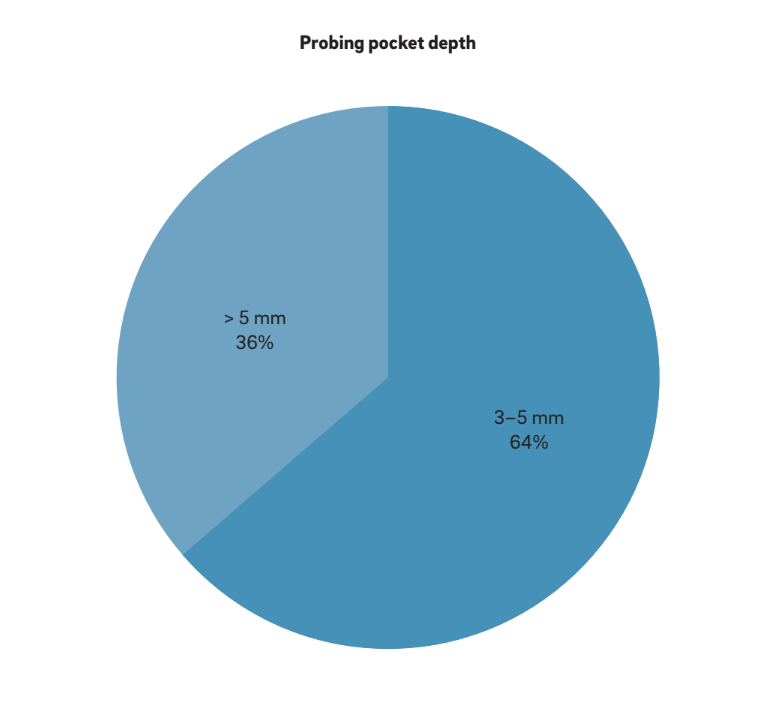
BOP и/или SUP были обязательными условиями во всех проанализированных исследованиях. В большинстве исследований для определения случаев использовались комбинации клинических и радиографических измерений. В двух проспективных исследованиях радиографический MBL не был представлен, и только клинические измерения использовались для оценки биологических осложнений. В этих случаях наличие BOP и/или SUP при зондировании и PPD ≥ 4 мм были обязательными условиями для диагностики периимплантита. В девяти исследованиях, включая одно рандомизированное контролируемое испытание, три проспективных и пять ретроспективных исследований, BOP и радиографические оценки проводились отдельно, без указания каких-либо измерений PPD. В этих случаях MBL в диапазоне от 0,5 мм до > 4 мм34 считался связанным с периимплантитом.
До 2012 года изменения уровня кристаллической кости либо не определялись, либо не сообщались четко, что затрудняло диагностику периимплантита. Однако даже в исследованиях, которые определяли сущность MBL, использовались разные диагностические критерии. В одном долгосрочном исследовании периимплантит определялся как наличие BOP, PPD ≥ 4 мм и MBL > 0,5 мм. Однако в другом исследовании использовалось MBL > 4 мм в качестве эталонного значения.34 Большинство исследований считали MBL > 2 мм для диагностики периимплантита. Ранее наша группа использовала радиографический MBL > 3 мм, полученный на базовом радиографическом снимке, сделанном в момент доставки протеза, для диагностики периимплантита. В трех других исследованиях MBL рассматривался в зависимости от времени, в течение которого протез находился в эксплуатации. Все исследования, кроме пяти, рассчитывали MBL в миллиметрах. В остальных исследованиях резьбы имплантата использовались в качестве эталона.
Восемь исследований применяли PPD > 5 мм для диагностики периимплантита. Marrone и др. определили периимплантит как наличие BOP, PPD > 5 мм и MBL > 2 мм. Charalampakis и др. применили критерии наличия BOP и/или SUP, PPD ≥ 5 мм и MBL ≥ 1.8 мм после одного года функционирования. Zetterqvist и др. включили случаи с PPD > 5 мм и MBL ≥ 3 мм. Два других исследования, одно проспективное и одно ретроспективное, применили наличие BOP и/или SUP, PPD > 5 мм и рентгенографические признаки MBL, не уточняя исходный уровень кости. Положительный BOP и/или SUP, рентгенографический MBL ≥ 3 мм и PPD ≥ 6 мм использовались Koldsland и др.
На 7-м и 8-м Европейском семинаре по пародонтологии периимплантный мукозит и периимплантит были описаны следующим образом: “изменения уровня кристаллической кости, наличие кровотечения при зондировании и/или супурации; с или без сопутствующего углубления периимплантных карманов.” Периимплантный мукозит был определен с положительным BOP и/или SUP, а периимплантит с положительным BOP и/или SUP в сочетании с рентгенографическим MBL ≥ 2 мм. Те же параметры использовали Zitzmann и Berglundh для определения периимплантита. Однако Atieh и др. использовали те же критерии, плюс PPD ≥ 5 мм, как определение периимплантита в своей систематической обзорной статье.
Обсуждение
Периимплантные заболевания проявляются в двух формах: периимплантный мукозит и периимплантит. Оба характеризуются воспалительной реакцией в ткани, окружающей имплантат. Периимплантный мукозит определен как обратимая воспалительная реакция в мягких тканях, окружающих функционирующий имплантат, тогда как периимплантит определен как более глубокое воспалительное поражение, характеризующееся углубленным периимплантным карманом и потерей поддерживающей кости вокруг функционирующего имплантата.
Исследования, опубликованные в начале 2010 года, предположили, что мукозит и периимплантит эквивалентны пародонтиту, поскольку оба описываются как дисбаланс между бактериальной нагрузкой и реакцией хозяина. Исходя из этого, оба заболевания тесно связаны с образованием биопленки, содержащей микробиоту, богатую грамотрицательными бактериями, в присутствии восприимчивого хозяина. Однако было показано, что микроорганизмы могут присутствовать, но не являются необходимыми для периимплантита. Кроме того, как пародонтит, так и периимплантит имеют несколько общих системных факторов риска или индикаторов (например, курение, плохая гигиена полости рта, диабет или история пародонтита, остеопороз). Аналогично, периимплантит, как и пародонтит, кажется, подвержен влиянию определенного генетического профиля (т.е. полиморфизма интерлейкина-1). Другие отвергли описание заболевания, сопоставимого с пародонтитом, из-за анатомических различий, существующих между пародонтальными и периимплантными структурами (например, различная ориентация коллагеновых волокон [перпендикулярная против горизонтальной], васкуляризация или способность к восстановлению, а также механическая устойчивость, обеспечиваемая пародонтальной связкой). На самом деле, пародонтит характеризуется воспалительным разрушением поддерживающего аппарата зубного ряда (пародонт), включая пародонтальную связку и альвеолярную кость. Из-за различного состава двух поддерживающих тканей подобные тканевые реакции вокруг имплантата и зуба кажутся крайне маловероятными. Термин "оссео-недостаточность" был предложен Зарбом и Кокой для описания различия между периимплантитом и потерей кости, вызванной пародонтитом. Анатомическая картина резорбции кости из-за пародонтита или периимплантита различается, во многих случаях очень широкие костные кратеры являются типичными для имплантата, но не для зуба. Следовательно, периимплантит можно считать отличным от пародонтита, поскольку он значительно отличается по началу и прогрессированию и имеет низкую предсказуемость лечения; следовательно, его лечение должно быть сосредоточено на ранней диагностике и контроле факторов риска или индикаторов, чтобы предотвратить его возникновение.
На сегодняшний день не существует стандартизированных параметров для клинического различения различных стадий и тяжести периимплантита. Критерии, используемые для диагностики периимплантита, остаются неопределенными. Большинство существующих исследований использовали клинические параметры в сочетании с рентгенографическими данными для определения периимплантита. Однако клинические параметры, такие как BOP и PPD вокруг имплантатов, менее предсказуемы, так как на них влияют большее количество сопутствующих факторов по сравнению с естественными зубами. Более того, любой фактор, способствующий образованию налета (например, плохая гигиена полости рта) или способности защиты организма (например, курение, чрезмерное употребление алкоголя, генетические особенности, история пародонтита или использование бисфосфонатов), может способствовать развитию периимплантита. Диагностика и прогрессирование периимплантита могут характеризоваться увеличением показателей клинических параметров (PPD, BOP, SUP или даже подвижности), MBL и микробиологии. Что касается клинических параметров, PPD является действительным методом оценки, так как существует корреляция между зафиксированными уровнями костной ткани и рентгенографической проникаемостью зонда. Тем не менее, в поперечном исследовании, измеренные во время операции уровни костной ткани вокруг имплантатов были более апикальными, чем рентгенографические уровни костной ткани. SUP встречается чаще у имплантатов с прогрессирующей потерей костной ткани, чем без нее, особенно у курильщиков, и может быть связан с эпизодами активного разрушения тканей. В систематическом обзоре Берглунд и др. определили периимплантит как наличие PPD ≥ 6 мм или MBL ≥ 2,5 мм. Ланг и Берглунд в консенсусе Европейской федерации пародонтологии 2011 года заявили, что клинические и рентгенографические данные должны регулярно собираться после установки протезов на имплантаты для установления базового уровня для диагностики периимплантита во время обслуживания пациентов с имплантатами. Метанализ Деркаса и Томаси четко показал положительную связь между распространенностью периимплантита и временем функции. Наличие потери костной ткани и PPD само по себе может быть недостаточно для установления диагноза периимплантита. Один важный фактор, который потенциально влияет на широкий диапазон распространенности периимплантита, - это отсутствие консенсуса относительно клинических параметров. Например, одно исследование сообщило, что если использовать PPD > 4 мм в качестве критерия, то 74,8% людей имели периимплантит, но если это измерение изменить на > 6 мм, то распространенность упала до 43,9%. Когда рентгенографический MBL рассматривался для определения периимплантита, 25,3% людей показали > 2 мм, в то время как 13,1% имели > 3 мм. Действительно, если учитывать PPD, можно обнаружить дальнейшую гетерогенность. Зондирование вокруг имплантатов зависит от многих факторов, таких как размер зонда, сила зондирования, направление зонда, здоровье и толщина мягких тканей вокруг имплантата, а также дизайн шейки имплантата и суперструктуры. Фактически, платформа с переключением, а также дефектные реставрации могут усложнять зондирование и, таким образом, скрывать истинный масштаб периимплантита. Более того, наличие несоответствий в уровнях жестких и мягких тканей в буколингвальной области может привести к различным показаниям PPD.
Из-за отсутствия стандартных параметров для определения наличия и степени тяжести периимплантита трудно разработать клиническую стратегию, основанную на PPD, для управления этой распространенной проблемой в имплантологии. Однако Фрум и Розен предложили классификационную систему для определения степени тяжести периимплантита на основе PPD, MBL и клинических признаков BOP и/или SUP,28 но эта система еще не была валидирована. Более того, в серии исследований Мерли и др. согласие между оценщиками при диагностике периимплантного заболевания оценивалось как лишь хорошее, из-за неясного определения периимплантита и мукозитов, при этом полное согласие было достигнуто только в половине случаев (52%).
Подавляющее большинство (45%) исследований, включенных в данный обзор, обнаружили радиографический MBL > 1–2 мм после протезирования. Следовательно, предлагаются следующие критерии для определения периимплантита: радиографический MBL > 1 мм после установки имплантата или 2 мм как минимум через шесть месяцев после установки имплантата как хороший индикатор периимплантита. BOP не обладает высокой предсказательной ценностью из-за слабой связи мягких тканей вокруг зубных имплантатов. Аналогично, PPD в значительной степени зависит от дизайна имплантата (уровень кости против уровня ткани), апикокорональной позиции и биотипа. Из извлеченных данных кажется логичным рассматривать радиографический MBL как самый унифицированный и точный индикатор периимплантита. Хотя пороговое значение зависит от воспалительного паттерна пациента, типа операции, апикокорональной позиции имплантата, макродизайна имплантата и кристального модуля, учитывая быстрое прогрессирование заболевания с течением времени, необходимо строгое радиографическое наблюдение, если обнаруживается какой-либо клинический симптом. Более того, клиницист должен использовать комбинацию множества доступных клинических параметров, таких как PPD, воспалительный статус слизистой, BOP при легком зондировании, радиографический MBL и, возможно, биомаркеры бактериальной и/или периимплантной крецикулярной жидкости для установления точного диагноза периимплантита. В отличие от случая с пародонтитом, бактериальные тесты могут быть ненадежными для диагностики периимплантита. Это предполагает, что экосистемы пародонта и периимплантита значительно различаются и, следовательно, периимплантное заболевание может не всегда рассматриваться как инфекционное заболевание. Аналогично, такое различие было показано в отношении патогенеза. Более того, не было найдено доказательств того, что первичная инфекция вызывала резорбцию краевой кости.
Заключение
Доступная научная литература предполагает отсутствие единого определения периимплантита. Актуальные определения периимплантита основывались исключительно на клинических параметрах без учета других потенциальных связанных факторов риска заболевания. Будущие исследования, применяющие последовательные определения случаев, должны быть рассмотрены.
Марко Талларико, Альберто Монье, Хом-Лай Ванг, Пабло Галиндo Морено, Эрта Ханарид и Луиджи Канулло
Ссылки
- Левиньяк Ж. [Периимплантационная остеолиз—периимплантоз—периимплантит]. Rev Fr Odontostomatol. 1965 Окт;12(8):1251–60. Французский.
- Хаммерле Х.Ч., Глаузер Р. Клиническая оценка лечения зубными имплантатами. Периодонтология 2000. 2004 Фев;34:230–9.
- Шварц Ф., Беккер К., Загер М. Эффективность профессионально проводимого удаления налета с или без дополнительных мер для лечения периимплантного мукозитиса. Систематический обзор и мета-анализ. J Clin Periodontol. 2015 Апр;42 Suppl 16:S202–13.
- Атиеh М.А., Альсабиха Н.Х., Фаджиоn К.М., Дункан У.Д. Частота периимплантных заболеваний: систематический обзор и мета-анализ. J Periodontol. 2013 Ноя;84(11):1586–98.
- Цитцманн Н.У., Марголин М.Д., Филиппи А., Вайгер Р., Крастль Г. Оценка пациента и диагностика в имплантационном лечении. Aust Dent J. 2008 Июн;53 Suppl 1:S3–10.
- Санз М., Чаппл И.Л.; Рабочая группа 4 VIII Европейского семинара по периодонтологии. Клинические исследования по периимплантным заболеваниям: консенсусный отчет Рабочей группы 4. J Clin Periodontol. 2012 Фев;39 Suppl 12:202–6.
- Американская академия периодонтологии. Отчет академии: периимплантный мукозит и периимплантит: текущее понимание их диагностики и клинических последствий. J Periodontol. 2013 Апр;84(4):436–43.
- Ланг Н.П., Берглунд Т.; Рабочая группа 4 Седьмого Европейского семинара по периодонтологии. Периимплантные заболевания: где мы сейчас?—Консенсус Седьмого Европейского семинара по периодонтологии. J Clin Periodontol. 2011 Мар;38 Suppl 11:178–81.
- Чан Х.Л., Лин Г.Х., Суарез Ф., Макичерн М., Ванг Х.Л. Хирургическое лечение периимплантита: систематический обзор и мета-анализ результатов лечения. J Periodontol. 2014 Авг;85(8):1027–41.
- Линдхе Й., Мейле Й.; Группа D Европейского семинара по периодонтологии. Периимплантные заболевания: консенсусный отчет Шестого Европейского семинара по периодонтологии. J Clin Periodontol. 2008 Сен;35(8 Suppl):282–5.
- Момбелли А., Мюллер Н., Чионка Н. Эпидемиология периимплантита. Clin Oral Implants Res. 2012 Окт;23 Suppl 6:67–76.