Внутрипротоковая хирургия слюнных желез пациентов после радиойодтерапии
Цель — описание и оценка методов диагностики и лечения сиалоаденита, развившегося после радиойодтерапии.
Материалы и методы. Проводились диагностика и лечение 28 пациентов с диагнозом «Хронический сиалоаденит или обострение хронического сиалоаденита». В диагностику входили опрос, осмотр, зондирование, ультразвуковое исследование с внеротовым датчиком, без стимулирования выработки слюны и диагностическая сиалоэндоскопия, при наличии обструктивной патологии протоковой системы проводилась лечебная сиалоэндоскопия.
Результаты. Клинические симптомы могли затрагивать различные слюнные железы, чаще всего поражению под- вергались околоушные слюнные железы с двух сторон (36%), а первичные проявления по данным анамнеза на-блюдались в период от 6 мес до года (35%). У 16 пациентов из 28 (57%) присутствовали структурные изменения как минимум одной слюнной железы. При ультразвуковой визуализации расширения протока во время сиалоэндоско-пии в 15 случаях из 28 (54%) определялась единичная стриктура протока. При сиалоэндоскопии обструктивные из-менения протоковой системы были представлены слизистыми бляшками, стенозами, стриктурами, которые могли быть единичными, множественными или тотальным сужением. При обнаружении протоковой обструкции проводи-лось ее устранение, восстанавливалась проходимость протока.
Заключение. С учетом развития малоинвазивных технологий и повышения чувствительности ультразвукового исследования необходимо дальнейшее изучение данной темы.
Введение
Радиойодтерапия является широко используемым методом лечения заболеваний щитовидной железы, особенно в случаях злокачественных новообразований. Целью лечения является удаление оставшейся ткани щитовидной железы после тиреоидэктомии. Молекулы I накапливаются в измененных тироцитах, что в конечном итоге приводит к их разрушению. При наличии злокачественных опухолей в щитовидной железе радиойодтерапия становится необходимой процедурой, которая значительно улучшает прогноз заболевания. Хотя этот метод обладает определенными преимуществами, он также сопряжен с риском формирования осложнений.
Способностью накапливать радиоактивный йод, помимо щитовидной железы, обладают многочисленные ткани и органы человека. К ним относятся слюнные железы, слизистая желудочно-кишечного тракта, гонады, молочная железа в период лактации. Включение I в клетки опосредуется симпортером йода и натрия. Из-за способности накопления йода слюнной железой могут происходить изменения паренхимы, приводящие к гипофункции, ксеростомии, дисфагии и сиаладениту.
Околоушная слюнная железа (ОСЖ) более подвержена радиационному воздействию, чем подчелюстная железа (ПСЖ), поскольку в основном состоит из серозных клеток, которые восприимчивее к радиации, чем другие клетки слюнных желез. В результате околоушные железы поражаются чаще, чем подъязычные и подчелюстные. После радиойодтерапии пациенты могут жаловаться на боль и припухлость в околоушной области, гипосаливацию, а также увеличение слюнных желез в разные периоды времени.
Методы диагностики этого осложнения могут быть различны. Ультразвуковая диагностика обычно используется для выявления характеристик стеноза, расширения протока, перегиба, мегадук-та и эхогенности. Сиалоэндоскопия применяется для оценки диаметра стенозированных и нормальных протоков, местоположения сужения, длины протока и типа ткани в пораженной области. При проведении сцинтиграфии авторы выявили пограничную дозовую активность в 5,55 ГБк, за пределами которой наблюдается снижение выработки слюны.
На сегодняшний момент в представленной лите ратуре нет сформированного алгоритма лечения слюнных желез после радиойодтерапии. Проводятся лишь попытки изучения использования массажа, парасимпатической стимуляции (пилокарпин), гипноза, генной терапии, инъекции защитного белка и сиалоэндоскопии в качестве методов расширения небольших стриктур и орошения протоков слюнных желез.
Цель
Цель нашего исследования — описание и оценка методов диагностики и лечения сиалоаденита, развившегося после радиойодтерапии.
На базе онкологического отделения No 8 (ЧЛХ) ФГБОУ ВО ПСПбГМУ им. академика И. П. Павлова проводилось лечение 28 пациентов с диагнозом хронического сиалоаденита или обострения хронического сиалоаденита.
Все медицинские исследования соответствуют Хельсинкской декларации о медицинских протоколах. Информированное согласие было получено от всех участников.
Для описания переменных, отражающих признаки, были использованы методы описательной статистики. На первом этапе статистического анализа произведена проверка количественных переменных на нормальность распределения с помощью теста Шапиро–Уилка. В том случае, когда данные подчинялись нормальному закону распределения, описательная статистика переменных производилась с помощью показателя среднего арифметического и стандартного отклонения (M±SD), когда данные не подчинялись нормальному распределению — с помощью медианы и межквартильного размаха (Me [Q25–Q75]). Статистическая обработка данных выполнялась с помощью пакета прикладных статистических программ MedCalc® (ver. 20.118) и с помощью программы Microsoft® Excel (ver. 16.16.12).
Среди 28 пациентов было 27 женщин (95,26%) и 1 мужчина (4,74%). Возраст пациентов варьировал от 21 до 77 лет, средний возраст составил 50,54±13,75 года (95% ДИ 45,20–55,87). Общие критерии включения пациентов в исследование:
- Пациенты должны пройти информирование и дать добровольное согласие в письменной форме на участие в клиническом исследовании.
- Пациенты поступали в клинику в экстренном или плановом порядке с диагнозом: обострение хронического / хронический сиалоаденит.
- В анамнезе пациентов имеется лечение радиоактивным йодом.
- Все пациенты должны были пройти комплексное обследование.
- Всем пациентам показаны лечебные мероприятия. Пациенты с ранее существовавшими заболевани-
ями слюнных желез были исключены. Проводилось стандартное клиническое исследование (опрос, осмотр, зондирование), а также ультразвуковое исследование с использованием аппарата (SonoScape S8Exp, Китай) с внеротовым датчиком, без стимулирования выработки слюны. Диагностическая сиалоэндоскопия выполнялась с помощью полужесткого эндоскопа (Karl Stortz, Германия) диаметром 1,1 и 1,6 мм.
При визуализации одной или множественных стриктур или стенозов сразу же проводилась лечебная сиалоэндоскопия с применением дилататоров устья протока, бужей, буров различного диаметра и катетера.
Результаты и обсуждение
Физиологическое поглощение йода, опосредованное симпортером натрия и йода, в слюнной железе обусловливает ее восприимчивость к повреждению, вызванному радиоактивным йодом, что может вылиться в развитие воспалительных процессов и ксеростомии.
В диагностике и лечении данной патологии важную роль играют первичные сведения. Проанализировав эти данные, возможно выявить особенности клинических проявлений. В 25 случаях из 28 (89,29%) пациенты получали радиойодтерапию по поводу злокачественного образования щитовидной железы и только в 3 случаях (10,71%) — по поводу другой патологии, например диффузного токсического зоба. Минимальная активность вводимого радиофармпрепарата составляла 2,56 ГБк, а максимальная – 5,82 ГБк, медиана суммарной дозы была 3,86 ГБк [3,50–4,00], причем двум пациентам из 28 (7%) процедура проводилась дважды.
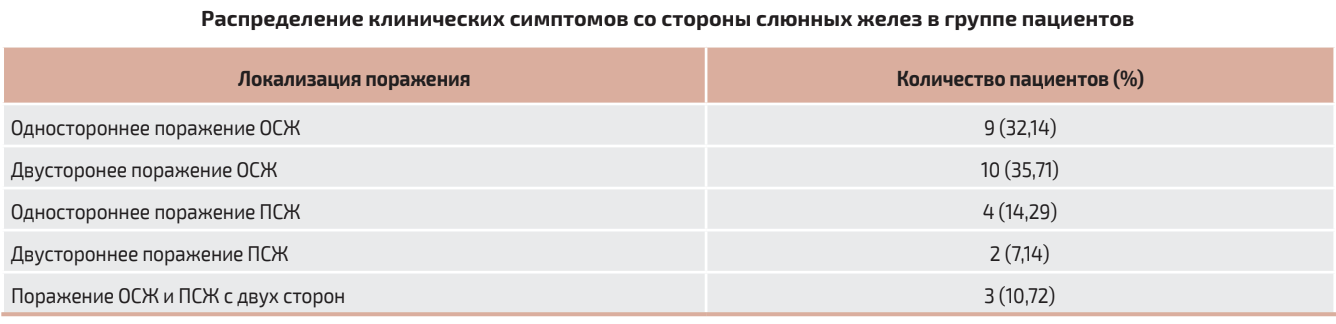
Клинические симптомы могли определяться в разных слюнных железах, поражение могло быть односторонним или двусторонним (табл. 1), а также про-являться в разные периоды времени. Поражения ОСЖ и ПСЖ с одной стороны не выявлено. Основными жалобами были увеличение слюнной железы (рис. 1), боль, чувство тяжести, сухость в полости рта.
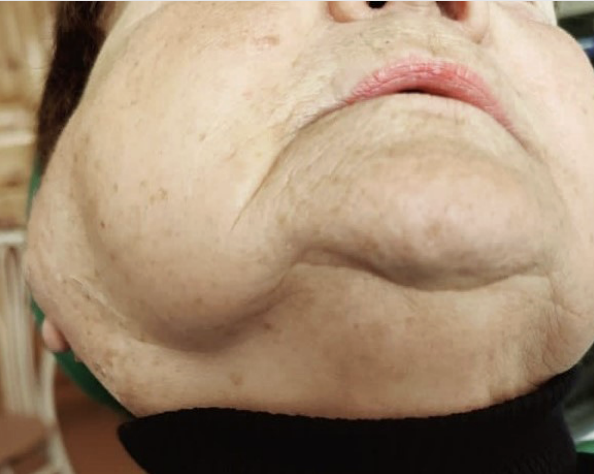
Все пациенты (n=28) были разделены по срокам возникновения первичных симптомов поражения больших слюнных желез:
• 1‐я группа, 8 (28,57%) — до 6 месяцев;
• 2‐я группа, 10 (35,71%) — от 6 месяцев до 1 года;
• 3‐я группа, 6 (21,44%) — от 1 года до 2 лет;
• 4‐я группа, 4 (14,28%) — позднее чем через 2 года.
Медиана времени от момента начала радиойодаблации (первого курса радиойодтерапии) до развития поражения слюнных желез составила 14,5 мес (95% ДИ 11,0–113,0).
Всем пациентам (n=28) проводилось ультразвуковое исследование всех больших слюнных желез. Визуализированы различные изменения: снижение эхогенности, неоднородность структуры, расширение протока, лимфаденопатия (рис. 2).
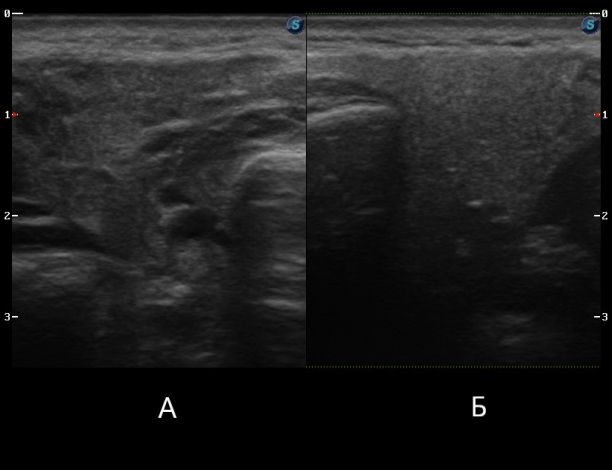
При оценке состояния слюнных желез было выявлено, что их поражение могло варьироваться от минимум одной железы до всех, так же как и количество изменений. Так, например, у одного пациента могло быть нарушение структуры околоушной слюнной железы и расширение протока подчелюстной слюнной железы. Однако не было выявлено ни одного пациента с изолированным повреждением подъязычной слюнной железы. При анализе данных мы не выявили закономерности тяжести патологических изменений, а также количества поврежденных слюнных желез от активности радиофармпрепарата. Однако в исследовании Е. Horvath с соавт. было выявлено, что самая значительная частота возможных повреждений (77,7%) слюнных желез может быть связана с активностью I 7400 МБк.
У 16 пациентов из 28 (57%) присутствовали структурные изменения как минимум одной слюнной железы.
Всем (n=28) проводилась диагностическая сиалоэндоскопия. Количество обследуемых слюнных желез зависело от наличия жалоб. Всего было исследовано 35 околоушных слюнных желез и 14 подчелюстных слюнных желез (табл. 2).
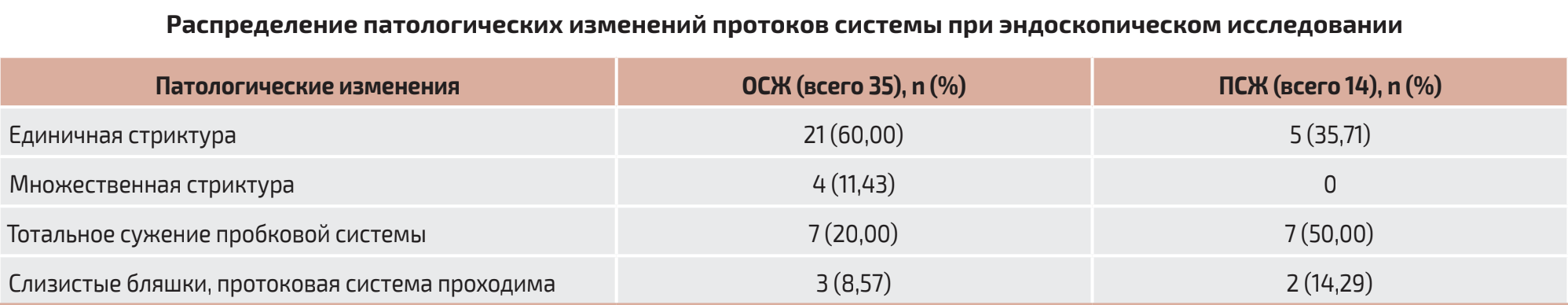
Также было выявлено, что при ультразвуковой визуализации расширения протока во время сиалоэндоскопии в 15 случаях из 28 (54%) определялась единичная стриктура протока околоушной или подчелюстной слюнной железы.
При визуализации единичных и множественных сужений во всех случаях проводилось их иссечение при помощи бура, а также установка катетера для профилактики повторного формирования стриктуры. При визуализации тотального сужения протоковой системы назначалась только симптоматическая терапия, направленная на уменьшение частоты воспалительных процессов в слюнной железе.
Заключение
На сегодняшний день диагностика и лечение патологии слюнных желез после радиойодтерапии не имеет четкого алгоритма. Не отработаны визуальные критерии поражения протоковой системы, которые могут дать обоснование методики выбора лечения и прогностическую успешность его. Поэтому данная тема остается актуальной и требует дальнейшего изучения.
Финансирование исследования и конфликт интересов.
Исследование не финансировалось каким-либо источником, и конфликты интересов, связанные с данным исследованием, отсутствуют.
Авторы
А. И. Яременко, А. Я. Разумова, Н. Л. Петров, С. И. Кутукова, А. Л. Вааз
Список литературы
- Бичев Р. О., Гайдук И. В., Панин А. М., Мкртумян А. М., Вар-танян К. Ф., Кириенко С. Л., Мирзоянц С. Г. Сиаладенит на фоне терапии радиоактивным йодом (Обзор литературы. Описание клинического случая). Российская стоматология 2015; 8(4): 19–24, https://doi.org/10.17116/rosstomat20158419–24. Bichev R. O., Gayduk I. V., Panin A. M., Mkrtumyan A. M., Vartanyan K. F., Kirien-ko S. L., Mirzoyants S. G. Sialadenitis during therapy with radioac-tive iodine-131. (Review of the literature. A case report). Rossiiskaya stomatologiya 2015; 8(4): 19–24, https://doi.org/10.17116/rossto-mat20158419–24.
- Коваленко В. А., Копчак А. В., Коваленко А. Е. Постлучевые си-алозоадениты у пациентов с папиллярными карциномами щито-видной железы. Вестник хирургии им. И. И. Грекова 2015; 174(1): 75–77, https://doi.org/10.24884/0042–4625–2015–174–1–75–77. Kova-lenko V. A., Kopchak A. V., Kovalenko A. E. Postradial sialozoadenitis in patients with papillary carcinoma of the thyroid gland. Vestnik khirur-gii im. I. I. Grekova 2015; 174(1): 75–77, https://doi.org/10.24884/0042–4625–2015–174–1–75–77.
- Tavares C., Coelho M. J., Eloy C., Melo M., da Rocha A. G., Pestana A., Batista R., Ferreira L. B., Rios E., Selmi- Ruby S., Ca-vadas B., Pereira L., Sobrinho Simoes M., Soares P. NIS expression in thyroid tumors, relation with prognosis clinicopathological and molecular features. Endocr Connect 2018; 7(1): 78–90, https://doi. org/10.1530/EC-17–0302.
- Krcalova E., Horacek J., Gabalec F., Zak P., Dolezal J. Scinti-graphic evaluation of salivary gland function in thyroid cancer patients after radioiodine remnant ablation. Eur J Oral Sci 2020; 128(3): 204–210, https://doi.org/10.1111/eos.12689.
- Stephens L. C., Schultheiss T. E., Price R. E., Ang K. K., Peters L. J. Radia-tion apoptosis of serous acinar cells of salivary and lacrimal glands. Cancer 1991; 67(6): 1539–1543, https://doi.org/10.1002/1097–0142(19910315)67:6< 1539:: aid-cncr2820670613>3.0.co;2-q.
- Abok K., Brunk U., Jung B., Ericsson J. Morphologic and histochem-ical studies on the differing radiosensitivity of ductular and acinar cells of the rat submandibular gland. Virchows Arch B Cell Pathol Incl Mol Pathol 1984; 45(4): 443–460, https://doi.org/10.1007/BF02889885.
- Goncalves M., Mantsopoulos K., Schapher M., Iro H., Koch M. Ul-trasound in the assessment of parotid duct stenosis. J Ultrasound Med 2019; 38(11): 2935–2943, https://doi.org/10.1002/jum.14999.
- Krcalova E., Horacek J., Gabalec F., Zak P., Dolezal J. Salivary gland function in thyroid cancer patients with radioiodine adminis-tration history. Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub 2020; 164(3): 277–283, https://doi.org/10.5507/bp.2019.023.
- Pascoe C., Duncan C., Lamb B. W., Davis N. F., Lynch T. H., Mur-phy D. G., Lawrentschuk N. Current management of radiation cys-titis: a review and practical guide to clinical management. BJU Int 2019; 123(4): 585–594, https://doi.org/10.1111/bju.14516.
- Horvath E., Skoknic V., Majlis S., Tala H., Silva C., Castillo E., Whittle C., Niedmann J. P., Gonzalez P. Radioiodine- induced salivary gland damage detected by ultrasonography in patients treated for papillary thyroid cancer: radioactive iodine activity and risk. Thyroid 2020; 30(11): 1646–1655, https://doi.org/10.1089/thy.2019.0563.