Возможности ультразвукового исследования в диагностике радиойодиндуцированного сиаладенита
Реферат. Хирургический подход является ведущим в лечении новообразований щитовидной железы. В ряде случаев лечения дифференцированного рака щитовидной железы после хирургического вмешательства необходимо применять радиойодабляцию с целью удаления оставшихся тиреоидных клеток или радиойодтерапию у пациентов группы промежуточного и неблагоприятного прогноза относительно риска прогрессирования. Наиболее высокую чувствительность к йоду после щитовидной железы имеют слюнные железы, накопление радиофармпрепарата в которых приводит к развитию сиаладенита. В настоящее время протокола диагностики для данного заболевания не существует.
Цель — изучить возможности ультразвуковой диагностики сиаладенита, ассоциированного с радиойодтерапией.
Материалы и методы. Проведено ретропроспективное исследование с анализом двух групп пациентов: I группа (n=30) с диагнозом сиаладенит, индуцированный терапией радиоактивным йодом, II группа (n=30) — группа здоровых добровольцев без патологии в челюстнолицевой области. Выполняли ультразвуковую диагностику состояния слюнных железы и сравнительный анализ полученных результатов.
Результаты. Было выделено 3 эхографических признака состояния слюнных желез при сиаладените после радиойодтерапии: изменение эхогенности, расширение протоковой системы слюнных желез, неоднородность структуры. Изменение эхогенности наиболее часто происходит в левой околоушной слюнной железе (ОСЖ) — 6,7%. У пациентов с поражением ОСЖ справа и слева показатель расширения протока составлял 7,5 и 6,7% соответственно (расширение до 3 мм). Неоднородность структуры слюнных желез наиболее часто проявлялась в левой ОСЖ — 10%.
Заключение. Метод ультразвуковой диагностики информативен, недлителен в выполнении и интерпретации данных, не имеет абсолютных противопоказаний, поэтому может быть первичным звеном в диагностике сиаладенита, развившегося на фоне радиойодтерапии.
Введение
По данным Национального института рака США, злокачественные новообразования щитовидной железы являются наиболее распространенной эндокринной онкопатологией, на ее долю приходится 2,2% всех случаев рака, ежегодно диагностируемых во всем мире. В последние годы происходит рост заболеваемости населения раком щитовидной железы (РЩЖ), и он превосходит рост заболеваний раком других локализаций, составляя 58%, особенно среди женщин (70% от всех случаев).
В настоящее время основным методом лечения дифференцированного РЩЖ является хирургический. В случае лечения пациентов группы высокого риска рецидива дифференцированного РЩЖ, а также с целью снижения риска метастазирования у больных группы промежуточного риска рецидива дифференцированного РЩЖ, возникающего в 15% случаев, и абляции всех оставшихся клеток после тиреоидэктомии используется терапия радиоактивным йодом (РЙТ).
К нежелательным эффектам после такого лечения относятся цистит, желудочнокишечные осложнения, гипоспермия, вторичные злокачественные новообразования, патологии слезоотводящей системы, аменорея, костномозговая депрессия, миелит и, наиболее частое, постлучевой сиаладенит. Пятилетняя, а по некоторым данным 10летняя общая выживаемость больных дифференцированным РЩЖ превышает 90%, поэтому одной из целей терапии является повышение качества жизни пациентов после перенесенных оперативного вмешательства и введения радиофармпрепарата (РФП). Хронический сиаладенит, развившийся на фоне проведенной РЙТ, проявляется в виде увеличения больших слюнных желез, болевого синдрома в околоушножевательных и подчелюстных областях и сухости в полости рта.
Эта патология не имеет протокола диагностики, а ультразвуковое исследование может стать первичным звеном в алгоритме постановки диагноза. Поэтому цель данной работы состоит в определении возможных изменений в больших слюнных железах под действием РФП при ультразвуковом исследовании. На базе онкологического отделения № 8 (челюстнолицевая хирургия) ПСПбГМУ им. акад. И.П. Павлова проводилось лечение 30 пациентов с диагнозом «хронический сиаладенит» (120 больших слюнных желез: подчелюстных и околоушных), которые составили I группу исследования.
Для определения так называемой диагностической нормы УЗ-картины паренхимы и протоковой системы слюнных желез была сформирована контрольная группа из 30 здоровых добровольцев без патологий в челюстнолицевой области, они составили II (контрольную) группу. В рамках первичной диагностики всем пациентам и здоровым добровольцам было проведено ультразвуковое исследование околоушных и поднижнечелюстных слюнных желез (ОСЖ и ПСЖ) (120 слюнных желез).
Исследование подъязычной слюнной железы не выполнялось в связи с невозможностью ее четкой визуализации на УЗ-аппарате. УЗИ проводили с использованием аппарата (Sono-Scape S8Exp, Китай) с внеротовым датчиком, без дополнительной стимуляции выделения слюны: околоушная и подчелюстная слюнные железы были осмотрены в поперечной и продольной плоскостях, проводилась оценка ткани паренхимы, диаметр протоковой системы измерялся в точке максимального расширения протока, выше упомянутых слюнных желез.
Научная гипотеза:
- H₀ — картина радиойодиндуцированного сиаладенита не имеет статистических УЗ-паттернов, частота и степень развития сиаладенита при проведении РЙТ зависит от накопленной дозы;
- H₁ — картина радиойодиндуцированного сиаладенита имеет статистические УЗ-паттерны, частота и степень развития сиаладенита при проведении РЙТ не зависит от накопленной дозы;
- α=0,05 — ошибка 1-го рода;
- β=0,8 — ошибка 2-го рода.
На первом этапе статистического анализа проведена проверка количественных переменных на нормальность распределения с помощью теста Шапиро—Уилка. Когда данные подчинялись нормальному закону распределения, описательная статистика переменных выполнялась с помощью показателя среднего арифметического и стандартного отклонения (M±SD), если данные не подчинялись нормальному распределению — с помощьюмедианы и межквартильного размаха (Me [Q₂₅—Q₇₅]). В I группе был всего 1 мужчина и 29 женщин в возрасте от 21 года до 77 лет, средний возраст составил 51,1±13,6 года (95% ДИ 46,0—56,2 года). II группу составили 12 мужчин и 18 женщин в возрасте от 21 года до 72 лет, медиана возраста — 25 лет [21—29 лет]. В I группе было значимо больше женщин, чем в контрольной группе (p=0,001), все участники II (контрольной) группы были значимо моложе, чем пациенты I группы (p<0,001). Из 30 пациентов I группы 27 получали РЙТ по поводу дифференцированного РЩЖ, 2 — по поводу диффУЗ-ного токсического зоба и 1 — по поводу многоУЗ-лового нетоксического зоба. Доза облучения, полученная пациентами основной группы, варьировала от 2,56 до 6,77 ГБк, медиана дозы РЙТ, после которой у пациентов этой группы развилось поражение слюнных желез, составила 3,86 ГБк [3,50—4,00 ГБк]. В исследование не включали пациентов с любыми нежелательными явлениями после радионуклидного лечения, не разрешившихся до I степени токсичности, определяемого по шкале CTCAE 5.0 (за исключением поражения слюнных желез). Также в исследование не включали пациентов и здоровых добровольцев с любыми сопутствующими состояниями в стадии суб и декомпенсации.
Результаты
При сиаладените на фоне РЙТ происходят такие изменения паренхимы и протоковой системы слюнных паттернах картины УЗИ: появление неоднородности структуры железы, снижение эхогенности и расширение протоковой системы (табл. 1, 2).
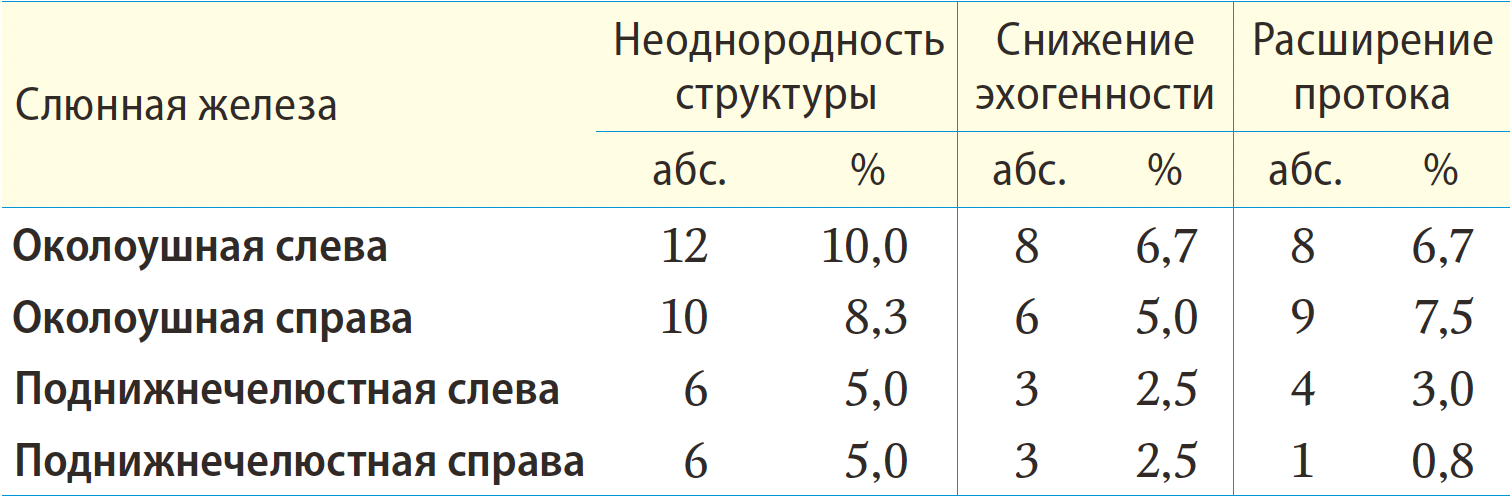
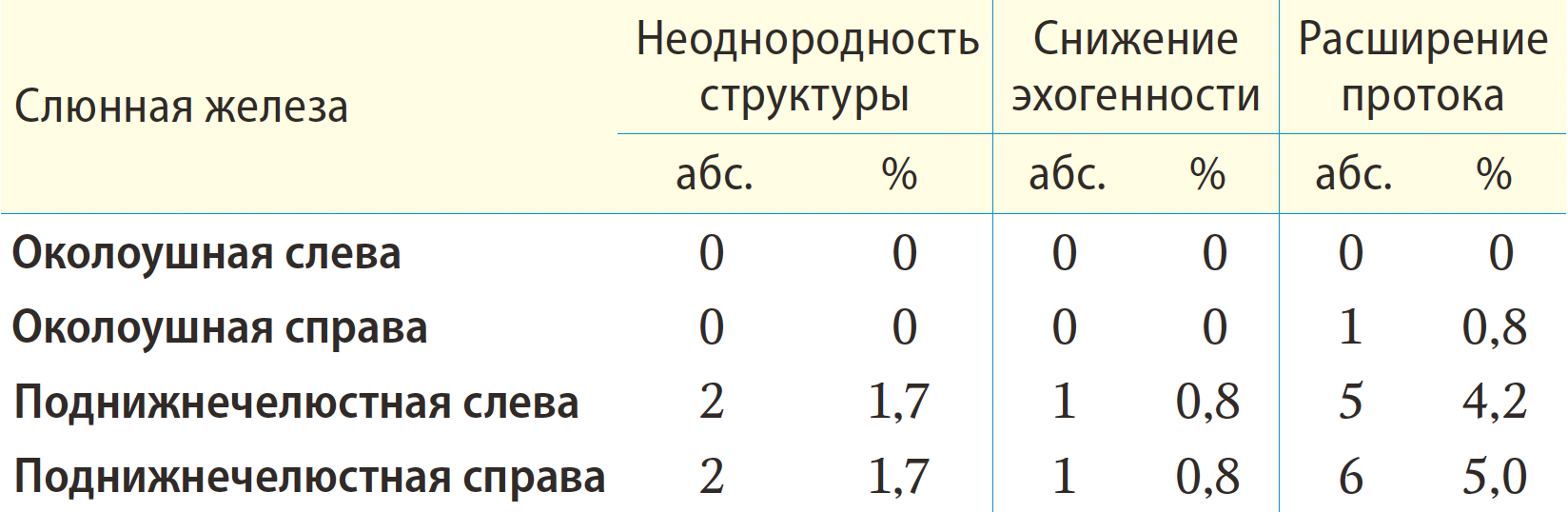
Эхогенность
У пациентов после радионуклидной терапии такие изменения имеются наиболее часто (6,7%) в левой ОСЖ. Неоднородность структуры железы может быть зарегистрирована у пациентов практически здоровых, без какихлибо клинических признаков поражения слюнных желез: в нашем исследовании в контрольной группе этот показатель составляет 0,83% в области каждой ПСЖ (см. табл. 2). Статистически достоверно значимой разницы между сторонами одних и тех же слюнных желез не выявлено у пациентов ни основной, ни контрольной группы (p=0,581 для ОСЖ, p=1,000 для ПСЖ). В основной группе изменение эхогенности было зарегистрировано одинаково часто и в ОСЖ, и в ПСЖ (p=0,123). В контрольной группе нарушение эхогенности без клинических признаков поражения СЖ чаще визуализировалось в ПСЖ (p=0,001). При сравнительном анализе частоты регистрации нарушения эхогенности между основной и контрольной группами, значимо чаще нарушение эхогенности выявлено у пациентов основной группы при анализе ОСЖ — p=0,004, при исследовании ПСЖ значимых различий не получено — p=0,312.
Расширение протока слюнной железы
У пациентов с поражением ОСЖ справа проявилось в 7,5% случаев, слева — у 6,7% пациентов, медиана расширения протока составила 2 мм [1,8—2,2 мм] при максимальном расширении до 3 мм (рис. 1).
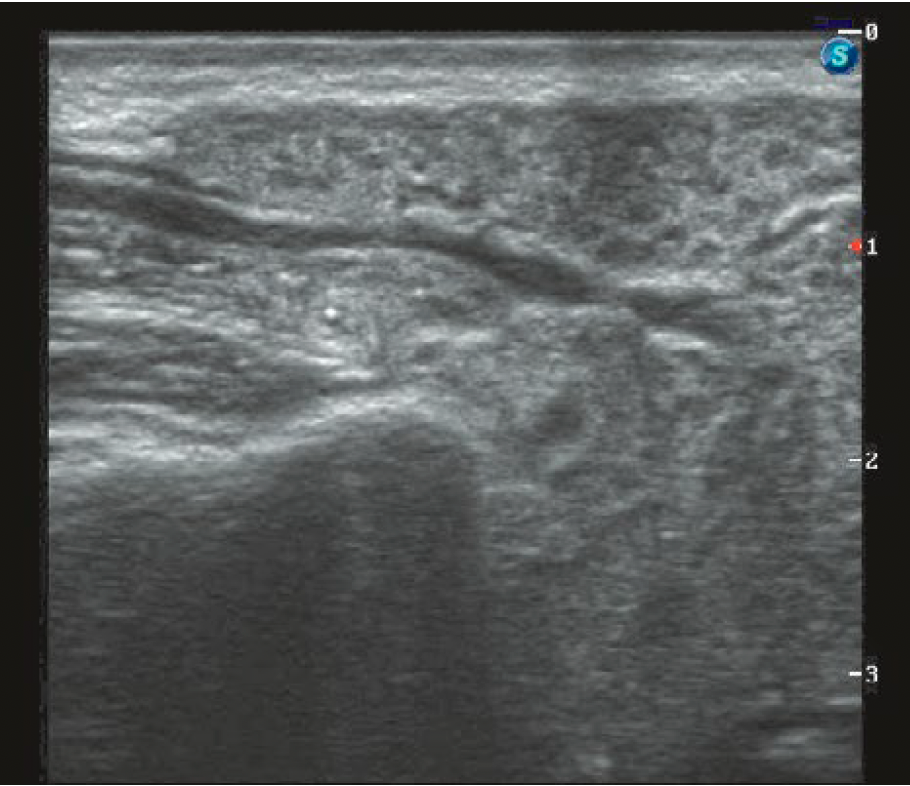
В контрольной группе этот показатель составляет в левой и правой ПСЖ по 4,2 и 5% соответственно, медиана расширения протока составила 0,5 мм [0,3—0,6] при максимальном расширении до 0,8 мм (рис. 2).
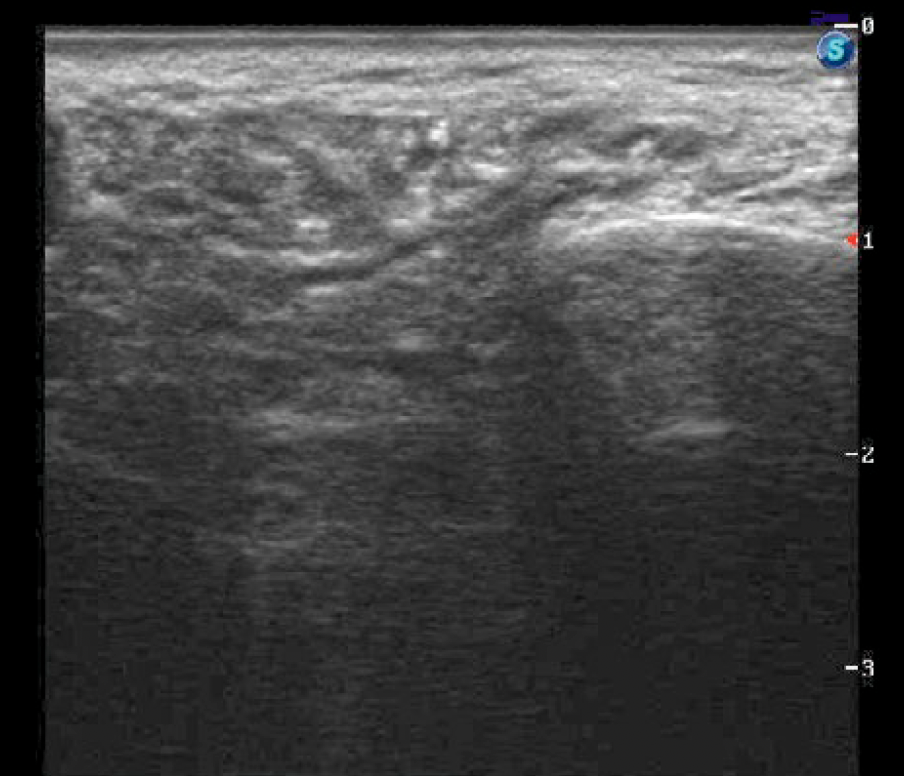
При сравнении степени расширения протоковой системы было отмечено более значительное расширение протоковой системы у пациентов после РЙТ в основной группе (p=0,003).
Неоднородность структуры
Неоднородность структуры является наиболее частым УЗ-паттерном, который можно обнаружить при УЗИ больших слюнных желез (p<0,001). У пациентов после радионуклидной терапии такие изменения чаще всего имеются в левой ОСЖ — 10%, в правой ОСЖ — 8%, в ПСЖ — 5%. В контрольной группе людей этот показатель не превышает 2% в области каждой ПСЖ. При сравнении частоты регистрации неоднородности структуры было выявлено значимо более частое наличие неоднородности в структуре ОСЖ после РЙТ (p<0,001), а в ПСЖ значимых различий не получено (p=0,151).
Обсуждение
Физиологически йодид, поступающий в организм, проникает в фолликулярные клетки за счет NaIсимпортера, осуществляющего транспорт через клеточную мембрану посредством электрохимического градиента, создаваемого NaKАТФазой. Этот процесс контролируется работой тиреотропного гормона. После множества биохимических реакций происходит образование гормонов тироксина и трийодтиронина.
Йод-131 применяется для тераностики в онкологии, т.е. для сканирования видимых введенных в организм пациента радиоизотопных индикаторов, а также для лечения злокачественных новообразований щитовидной железы. Таким образом, йод-131 из кровеносного русла поступает в фолликулярные клетки за счет действия NaIсимпортера. Именно эта способность ткани щитовидной железы поглощать и накапливать радиоактив ный йод, вследствие чего происходит выброс βчастиц и гибель клеток или лишь кумуляция йода, является основой применения РЙТ и радиойоддиагностики в работе с болезнью Грейвса, нетоксическим многоузловым, токсическим диффузным зобом и новообразованиями щитовидной железы.
Механизм образования нежелательных эффектов терапии йодом-131 объясняется наличием NaIсимпортера и в других органах: в слюнных железах (в протоковых эпителиальных клетках), в желудке (в муцинсекретирующих клетках), в молочной железе в период лактации (в альвеолярных клетках), а также в меньшем количестве в прямой, толстой и тонкой кишке, в поджелудочной железе, в почках, легких, плаценте, яичниках, в слезных железах, семенниках, предстательной железе, надпочечниках, вилочковой железе, гипофизе, сердце и в желчных протоках, вызывая образование хронических неспецифических воспалительных заболеваний и блокирование протоковых систем, например вторичная приобретенная вследствие лечения йодом-131 обструкция слезных путей.
Патология слюнных желез является одним из самых частых осложнений РЙТ — до 67% в случаев острых сиаладенитов, до 43% в случае хронических. Гибель клеток ацинусов слюнных желез обусловлена теми же механизмами, которые происходят в щитовидной железе, вследствие чего развивается острый или хронический сиаладенит с прогрессирующей обструкцией и ксеростомией. Более склонны к асептическому воспалению, а соответственно более часто поражаемые слюнные железы по клинической картине и данным УЗ-диагностики — околоушные, так как они состоят преимущественно из белковых клеток. Йод-131 накапливается, оседает и вызывает воспаление в большей степени в серозных и протоковых клетках по сравнению со слизистыми.
Поэтому клинически мы наблюдаем сухость в полости рта, вызванную уменьшением количества слюны и застоем ее изза образования стенозов и стриктур в протоковой системе, которые уже компенсаторно способствуют образованию расширений протоков, визуализируемых с помощью УЗ-диагностики.
Согласно клиническим рекомендациям, действующим с 2020 г. по настоящее время, существуют определенные критерии, по которым пациентов с дифференцированным РЩЖ первично относят к группам низкого, промежуточного и высокого риска. Следуя этому распределению, индивидуальному анамнезу, выбору масштаба оперативного вмешательства (возможные варианты тиреодэктомии взаимосвязаны с решением о послеоперационной РЙТ), врач определяет необходимую дозу РФП для конкретного пациента.
Кроме того, в рекомендациях есть описание диеты, которую необходимо соблюдать больному перед РЙТ, показания для ее проведения и исследования, рекомендуемые для выполнения перед радиойодабляцией/РЙТ. Но вариантов нежелательных эффектов и их предупреждения, кроме употребления лимона или жевательной резинки, после введения йода-131 нет. Однако данная рекомендация противоречива, так как раннее начало употребления сиалогов (например, лимонных конфет), а именно до 24 часов после введения РФП, по данным K. Nakada и соавт., только способствует возникновению осложнений со стороны слюнных желез за счет увеличения не только слюноотделения, но и притока крови к слюнных железам, а следовательно, и повышения уровня йод-131. Через 24 часа поглощение радиойода чувствительными к нему тканями выходит на стадию плато, поэтому в дальнейшем применение сиалогов носит положительный эффект.
Помимо лимонных конфет, в профилактике радиойодного сиаладенита возможно применение резерпина, амифостина , жевательных резинок, местного массажа, витамина E, хотя все же и в настоящее время нет единогласного решения об эффективном и действенном предотвращении возникновения осложнений терапии радиойодом на слюнные железы и лечения их.
По мнению E. Horvath и соавт., A. Sánchez Barrueco и др. имеется корреляция между дозой введенного РФП и риском возникновения сиаладенита. По нашим данным, а также по данным R.K. Thorpe и соавт. (2021), I.T. Lee и соавт., точной корреляции нет, так как из группы пациентов (n=30) с диагнозом «хронический сиаладенит/обострение хронического сиаладенита на фоне радиойодтерапии» наибольшее количество пораженных слюнных желез наблюдалось при дозе 4,0 ГБк.
Помимо отсутствия вышеописанной корреляции, мы не отметили взаимосвязи между введенной дозой йода131 и временем возникновения первых жалоб пациентов на патологию слюнных желез. Наименьший период времени с введения РФП до появления симптомов радиойодного сиаладенита составил 2 месяца и 17 дней при введении 2,56 ГБк, а наибольший — 9 лет 5 месяцев и 2 дня при введении 3,5 ГБк. Самое частое время возникновения клинических признаков повреждения слюнных желез составило от 6 месяцев до 1 года — 36,67%, что подтверждается данными R.K. Grewal и соавт. (2009).
Полученные нами критерии диффузных изменений эхогенности в сторону ее уменьшения и увеличения неоднородности структуры были выявлены во всех симптоматически вовлеченных в процесс воспаления слюнных железах, причем доза введенного РФП не влияла на количество пораженных слюнных желез и тяжесть патологических изменений.
Выводы:
- Ультразвуковая диагностика является информативным и эффективным методом первичной диагностики поражения слюнных желез у пациентов, получающих терапию радиоактивным йодом.
- Можно выделить 3 УЗ-паттерна при оценке патологии слюной железы после РЙТ:
- однородность структуры
- расширение протока
- эхогенность слюнной железы.
Таким образом, снижение эхогенности, появление неоднородности структуры, особенно ОСЖ, и расширение протоковой системы >0,8 мм являются значимыми УЗ-паттернами развития сиаладенита после РЙТ.
- Срок возникновения первых симптомов вариабелен, но зачастую он варьирует от 6 месяцев до 1 года.
- Наиболее часто регистрируется УЗ-признаки поражения ОСЖ в сравнении с подчелюстными.
- Ультразвуковое исследование должно стать первичным звеном при диагностике радиойодного сиаладенита, так как ни один из 60 человек не отказался от проведения УЗ-диагностики изза таких преимуществ метода, как отсутствие инвазивности, лучевой нагрузки, высокая скорость при проведении манипуляции и интерпретации данных, отсутствие противопоказаний к выполнению данного типа диагностики.
Авторы
А.Я. Разумова, Н.Л. Петров, А.Л. Вааз, А.И. Яременко, С.И. Кутукова, Е.В. Бородавина
Список литературы
Cronin K.A., Ries L.A., Edwards B.K. The surveillance, epidemiology, and end results (SEER) program of the National Cancer Institute. — Cancer. — 2014; 120 Suppl 23: 3755—7. PMID: 25412387
- Kitahara C.M., Sosa J.A. The changing incidence of thyroid cancer. — Nat Rev Endocrinol. — 2016; 12 (11): 646—653.
PMID: 27418023 - Иванов В.К., Горский А.И., Полькин В.В., Андреев В.Г., Кащеев В.В., Туманов К.А., Иванов С.А., Каприн А.Д. Динамика заболеваемости раком щитовидной железы населения России: основные факторы риска. — Радиация и риск (Бюллетень Национального радиационноэпидемиологического регистра). —2022; 4: 6—20. [Ivanov V.K., Gorski A.I., Polkin V.V., Andreev V.G., Kashcheev V.V., Tumanov K.A., Ivanov S.A., Kaprin A.D. Dynamics of thyroid cancer incidence in the population of Russia: main risk factors. — Radiation and Risk. — 2022; 4: 6—20 (In Russian)]. eLibrary ID: 50081784
- Deng Y., Li H., Wang M., Li N., Tian T., Wu Y., Xu P., Yang S., Zhai Z., Zhou L., Hao Q., Song D., Jin T., Lyu J., Dai Z. Global burden of thyroid cancer from 1990 to 2017. — JAMA Netw Open. — 2020; 3 (6): e208759. PMID: 32589231
- Jin Y., Van Nostrand D., Cheng L., Liu M., Chen L. Radioiodine refractory differentiated thyroid cancer. — Crit Rev Oncol Hematol. — 2018; 125: 111—120. PMID: 29650270
- Евтушенко А.В., Горчица Я.Ю., Сизов П.А., Смирнов А.А. Современная тактика хирургического лечения рака щитовидной железы. — European Science. — 2018; 4 (36): 80—89. [Evtushenko A.V., Gorchitsa Y.Y., Sizov P.A., Smirnov A.A. Modern tactics of treatment the cancer of thyroid gland. — European Science. — 2018; 4 (36): 80—89 (In Russian)]. eLibrary ID: 34913351
- Tsur N., Avishai G., Alkan U., Hod R., Shpitzer T., Bitton E., Gilat H. Ultrasonographic features of salivary glands after radioiodine therapy in patients with thyroid cancer. — Laryngoscope. — 2023; 133 (5): 1271—1275. PMID: 36354236
- Фархутдинова Л.М. Радиойодтерапия папиллярного рака щитовидной железы, осложненная лучевым миелитом. Клинический случай. — Архивъ внутренней медицины. — 2018; 3 (41): 223—230.
[Farkhutdinova L.M. Radioiodine therapy of papillary thyroid cancer, complicated by a radial myelitis. Clinical case. — The Russian Archives of Internal Medicine. — 2018; 3 (41): 223—230 (In Russian)]. eLibrary ID: 35002927 - Boucai L., Zafereo M., Cabanillas M.E. Thyroid cancer: A review. — JAMA. — 2024; 331 (5): 425—435. PMID: 38319329
- Tran T.V., Rubino C., Allodji R., Andruccioli M., Bardet S., Diallo I., Dottorini M., Garsi J., Hall P., HenryAmar M., Lamart S., Le Thai F., Lönn S., Ricard M., Schvartz C., Schlumberger M., Journy N., de Vathaire F. Breast cancer risk among thyroid cancer survivors and the role of I131 treatment. — Br J Cancer. — 2022; 127 (12): 2118—2124. PMID: 36224404
- Цомартова Д.А., Черешнева Е.В., Иванова М.Ю., Пашин С.С., КУЗ-нецов С.Л. Роль Na+/− симпортера в патологии щитовидной железы неопухолевого генеза. — Медицинский вестник Северного Кавказа. — 2019; 1—1: 131—134.
[Tsomartova D.A., Chereshneva Ye.V., Ivanova M.Yu., Pashin S.S., Kuznetsov S.L. Impact of Na+/− symporter to nononcologic pathology of the thyroid. — Medical News of North Caucasus. — 2019; 1—1: 131—134 (In Russian)]. eLibrary ID: 37634577 - Yavuz S., Puckett Y. Iodine131 uptake study. — StatPearls, 2025. PMID: 32644709
- Джикия Е.Л., Авилов О.Н., Киселева Я.Ю., Кулинич Т.М., Боженко В.К. Na+/I симпортер (NIS): структура, функции, экспрессия в норме и опухолях. — Вестник Российского научного центра рентгенорадиологии. — 2018; 1: 3. [DzhikiyaE.L., AvilovO.N., KiselevaYa.Yu., KulinichT.M., Bozhenko V.K. Sodium/iodide symporter (NIS): structure, function and role in in thyroid diseases. — Vestnik of the Russian Scientific Center of Roentgenoradiology. — 2018; 1: 3 (In Russian)]. eLibrary ID: 35121876
- КарпищенкоС.А., БелдовскаяН.Ю., БаранскаяС.В., Карпов А.А. Результаты эндоскопической эндоназальной дакриоцисториностомии в лечении вторичной приобретенной обструкции носослезного канала, возникшей после терапии радиоактивным йодом. — Практическая медицина. — 2018; 5: 23—27. [Karpishchenko S.A., Beldovskaya N.Yu., Baranskaya S.V., Karpov A.A. Outcomes of endoscopic endonasal dacryocystorhinostomy in the treatment of secondary acquired nasolacrimal duct obstruction after radioiodine therapy. — Practical medicine. —2018; 5: 23—27 (In Russian)]. eLibrary ID: 35653615
- AuttaraAtthakorn A., Sungmala J., Anothaisintawee T., Reutrakul S., Sriphrapradang C. Prevention of salivary gland dysfunction in patients treated with radioiodine for differentiated thyroid cancer: A systematic review of randomized controlled trials. —Front Endocrinol (Lausanne). — 2022; 13: 960265. PMID: 36105397
- Adramerinas M., Andreadis D., Vahtsevanos K., Poulopoulos A., PazaitouPanayiotou K. Sialadenitis as a complication of radioiodine therapy in patients with thyroid cancer: where do we stand? —Hormones (Athens). — 2021; 20 (4): 669—678. PMID: 34143403
- Костяева М.Г., Еремина И.З., Кастыро И.В. Морфология и физиология слюнных желез. — Голова и шея. — 2022; 3: 81—87. [KostyaevaM.G., EreminaI.Z., KastyroI.V. Morphology and physiology of the salivary glands. — Head and Neck. — 2022; 3: 81—87 (In Russian)]. eLibrary ID: 49444613
- Яременко А.И., Разумова А.Я., Петров Н.Л., Кутукова С.И., Вааз А.Л. Внутрипротоковая хирургия слюнных желез пациентов после радиойодтерапии. — Медицинский альманах. — 2023; 2 (75): 89—93. [Yaremenko A.I., Razumova A.Ya., Petrov N.L., Kutukova S.I., Vaaz A.L. Intraductal salivary gland surgery after radioiodine therapy. — Medical Almanac. — 2023; 2 (75): 89—93 (In Russian)]. eLibrary ID: 54126164
- Nakada K., Ishibashi T., Takei T., Hirata K., Shinohara K., Katoh S., Zhao S., Tamaki N., Noguchi Y., Noguchi S. Does lemon candy decrease salivary gland damage after radioiodine therapy for thyroid cancer? —J Nucl Med. — 2005; 46 (2): 261—6. PMID: 15695785
- Bohuslavizki K.H., Brenner W., Klutmann S., Hübner R.H., Lassmann S., Feyerabend B., Lüttges J., Tinnemeyer S., Clausen M., Henze E. Radioprotection of salivary glands by amifostine in highdose radioiodine therapy. — J Nucl Med. — 1998; 39 (7): 1237—42. PMID: 9669401
- Levy H.A., Park C.H. Effect of reserpine on salivary gland radioiodine uptake in thyroid cancer. — Clin Nucl Med. — 1987; 12 (4): 303—7. PMID: 3581610
- Haghighatafshar M., Nowshad R., Etemadi Z., Ghaedian T. The effect of chewinggum on dose rate of salivary gland in differentiated thyroid carcinoma patients treated with radioiodine. — Q J Nucl Med Mol Imaging. — 2020; 64 (3): 321—325. PMID: 29696945
- Horvath E., Skoknic V., Majlis S., Tala H., Silva C., Castillo E., Whittle C., Niedmann J.P., González P. Radioiodineinduced salivary gland damage detected by ultrasonography in patients treated for papillary thyroid cancer: Radioactive iodine activity and risk. — Thyroid. — 2020; 30 (11): 1646—1655. PMID: 32370663
- Sánchez Barrueco A., González Galán F., Alcalá Rueda I., Santillán Coello J.M., Barrio Dorado M.P., Villacampa Aubá J.M., Escanciano Escanciano M., Llanos Jiménez L., Mahillo Fernández I., Cenjor Español C. Incidence and risk factors for radioactive iodineinduced sialadenitis. — Acta Otolaryngol. — 2020; 140 (11): 959—962. PMID: 32815758
- Thorpe R.K., Foggia M.J., Marcus K.S., Policeni B., Maley J.E., Hoffman H.T. Sialographic analysis of radioiodineassociated chronic sialadenitis. — Laryngoscope. — 2021; 131 (5): E1450—E1456. PMID: 33200832
- Lee I.T., Chen W., Chen Q., Cole H.A., Bischoff L.A., Jessop A.C., Sobel R.K. Factors associated with radioactive iodine therapyacquired nasolacrimal duct obstruction. — Endocr Pract. — 2022; 28 (12): 1210—1215. PMID: 35970353
- Grewal R.K., Larson S.M., Pentlow C.E., Pentlow K.S., Gonen M., Qualey R., Natbony L., Tuttle R.M. Salivary gland side effects commonly develop several weeks after initial radioactive iodine ablation. — J Nucl Med. — 2009; 50 (10): 1605—10. PMID: 19759114
