Клиническое применение лазера Er,Cr:YSGG в эндодонтической терапии
Машинный перевод
Оригинальная статья написана на языке EN (ссылка для ознакомления) .
Полное устранение бактерий из инфицированных систем корневых каналов остается самой важной целью эндодонтической терапии. Однако, несмотря на множество новых продуктов и техник, достижение этой цели продолжает ускользать от нашей профессии. Исторически эндодонтическое лечение сосредоточивалось на дезинфекции корневых каналов с «захоронением» оставшихся бактерий в дентинных канальцах и недоступных областях системы корневых каналов. Хотя многие факторы были вовлечены в этиологию эндодонтических неудач, стало очевидно, что эти «захороненные» бактерии играют ключевую роль в сохранении эндодонтической болезни.
Хотя впечатляющие результаты были получены in vitro, энергия лазера сама по себе не смогла достичь полного уничтожения бактерий в удаленных зубах. С клинической точки зрения очевидно, что требуется комбинация различных методов лечения для стерилизации систем корневых каналов. Кроме того, существует множество клинических препятствий, которые дополнительно усложняют способность клинициста достичь этой цели. К ним относятся, но не ограничиваются: ограниченный эндодонтический доступ, сложная анатомия корневых каналов, ограничения методов орошения и инструментирования, неспособность захоронить бактерии и неспособность достичь и устранить бактерии глубоко в структуре зуба.
Хотя цель этой статьи заключается в том, чтобы сосредоточиться на клиническом использовании лазера Er,Cr:YSGG с радиальными насадками, необходимо иметь четкий протокол лечения, чтобы уменьшить бактериальную нагрузку внутри канала перед использованием лазера и облегчить доставку лазерной энергии в наиболее критическую часть корневого канала, апикальную треть.
Лазер эрбия, легированный хромом, иттрия, скандия, галлия и граната (Er,Cr:YSGG) излучает на длине волны 2,780 нм и сильно поглощается водой. Чем меньше глубина проникновения в воду или ткань (или чем выше поглощение), тем больше способность лазера резать или аблировать ткань (Рис. 1). Поскольку эта длина волны очень близка к максимуму поглощения воды в гидроксиапатите, фотоиабляция происходит там, где вода мгновенно испаряется, тем самым аблируя окружающую ткань. Гордона и др. обнаружили, что возможно достичь расширения и коллапса внутритрубочной воды на глубину до 1,000 мкм и более. Это поглощение, вызванное микропульсом, было способно производить акустические волны, достаточно сильные, чтобы разрушать и убивать внутритрубочные бактерии.
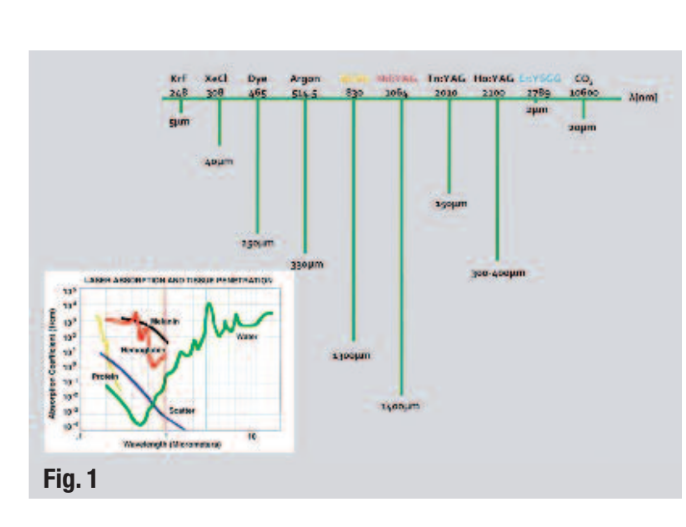
Эти результаты имеют значение, так как бактерии были обнаружены на глубине 1000 мкм, а E. faecalis на глубине 800 мкм. Ирриганты, такие как гипохлорит натрия, имеют ограниченное воздействие на эти бактерии с глубиной проникновения всего 100 мкм. Недавно было установлено, что увеличение концентрации, времени воздействия и температуры улучшает проникновение NaOCl.
Обещающие показатели уничтожения бактерий с использованием лазера Er,Cr:YSGG с радиальными наконечниками были зарегистрированы в удаленных зубах. Снижение уровня дезинфекции на 99,7% было достигнуто для E. faecalis на глубине 200 мкм в дентине и 94,1% (1 лог) на глубине 1,000 мкм.
Разработка радиального лазерного наконечника (Biolase Technology, Inc.) с формой наконечника, который излучает лазерную энергию в виде широкого конуса, позволяет лучше покрывать стенки корневого канала, чем наконечники с фронтальным излучением (Рис. 2). Это облегчает проникновение излучаемой лазерной энергии в дентинные канальцы, достигая бактерий, которые проникли глубоко в дентин.
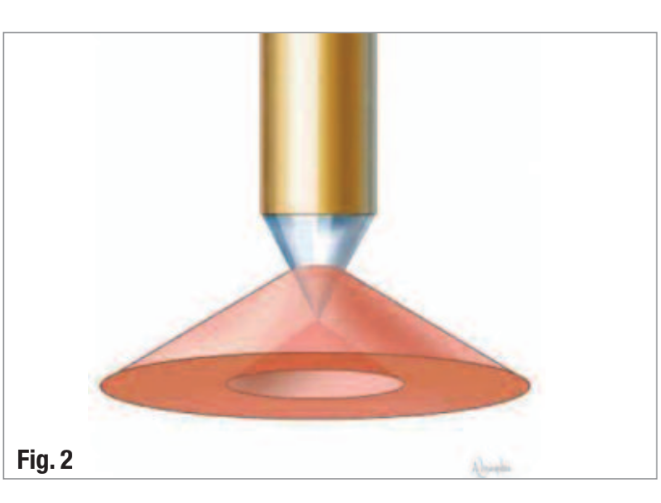
Протокол лечения
Современные методы, включающие ручные и/или ротационные инструменты, ирригацию с положительным давлением, с или без звуковой и ультразвуковой агитации, не обеспечивают полной дезинфекции канала. Протокол лечения, представленный в этой статье, включает три основных компонента: управление рабочей шириной корневого канала, ирригацию с отрицательным давлением на апексе и лазерную терапию внутри канала.
Управление рабочей шириной
Рабочая ширина (WW) корневого канала — это диаметр канала непосредственно перед его апикальной сужающейся частью. Аллен обнаружил, что 97 % каналов, не очищенных до их WW, имели остаточные загрязнения в критической апикальной области, в то время как 100 % тех, которые были очищены до их WW, были свободны от загрязнений на расстоянии 1 мм от апикальной сужающейся части. Исследования показали, что нам необходимо очищать до больших размеров, чтобы удалить бактерии и загрязнения. Обычные конусные файлы не могут этого достичь, не перемещая канал, создавая полосовые перфорации, ослабляя зуб или отделяя инструменты. Файл LightSpeed LSX (Discus Dental) является уникальным, чрезвычайно гибким, безконусным инструментом из NiTi, способным очищать до WW. Финальный апикальный размер — это размер инструмента, который завершает подготовку WW и определяется, когда файл LSX застревает на расстоянии 4 мм (или более) от рабочей длины (WL) и требует сильного нажатия для достижения WL. Индивидуально подготовленные апикальные участки критически важны для предсказуемо успешной эндодонтии и предоставляют значительные преимущества:
- эффективное удаление инфицированного материала, мусора, воспаленной и некротической ткани из апикальной области;
- позволяет разместить ирригирующую иглу на рабочей длине для апикальной ирригации с отрицательным давлением;
- облегчает размещение медикаментов внутри канала глубже в канале;
- и облегчает размещение лазерного наконечника с радиальным выстрелом на расстоянии 1 мм от рабочей длины.
Апикальная ирригация с отрицательным давлением
Существует две основные причины, по которым ирригаторы не достигают критических последних 3 мм корневого канала. Во-первых, при использовании ирригации с положительным давлением с иглой с боковым вентиляцией происходит мало промывания за пределами глубины иглы. Большая часть ирригатора следует по пути наименьшего сопротивления и выходит из канала, при этом апикальное промывание проникает только на 1-2 мм апикально от конца иглы. Для достижения эффективного апикального промывания наконечник иглы должен быть размещен на расстоянии 1 мм от рабочей длины, что значительно увеличивает риск несчастного случая с гипохлоритом натрия.
Во-вторых, наличие апикального парового замка из воздуха, trapped в канале, а также аммиака и углекислого газа, выделяющихся в результате растворяющего действия гипохлорита натрия на пульпную ткань, препятствует проникновению ирригантов в апикальную треть. Этот паровой замок нельзя удалить с помощью ручных или ротационных файлов, а также с помощью соников или ультразвуковой активации. В недавнем исследовании паровой замок привел к «значительному накоплению остатков и следов размазывания» в апикальных 0,5 до 1,0 мм закрытых систем корневых каналов.
EndoVac (Discus Dental) — это настоящая система ирригации с отрицательным давлением в апикальной области, которая обеспечивает непрерывную, высокообъемную ирригацию свежими жидкостями до терминала канала с одновременной эвакуацией. Она состоит из главного доставочного наконечника (Рис. 3), который подает жидкость в пульповую камеру, и макро- и микро-канюли (Рис. 4), которые отводят жидкость из камеры к терминалу канала путем эвакуации.
Эта система устраняет паровой замок и обеспечивает превосходную очистку, дезинфекцию и удаление смывного слоя, практически исключая угрозу несчастного случая с гипохлоритом натрия. По сравнению с ирригацией под положительным давлением с помощью иглы ProRinse, EndoVac обеспечил каналы, которые были на 366% и 671% чище на расстоянии 1 и 3 мм от рабочего уровня соответственно.
Когда EndoVac использовался в сочетании с инструментами LightSpeed LSX, каналы были на 99 и 99,5 % свободны от остатков на расстоянии 1 и 3 мм от рабочего длины, соответственно.
Лазерная терапия внутриканально
Заключительный этап подготовки и дезинфекции корневого канала завершается с помощью лазера Waterlase MD (Er,Cr:YSGG) с использованием радиально-стреляющих наконечников (Biolase Technology).
Лазерные наконечники доступны в двух размерах: RFT2 и RFT3 с диаметрами 275 и 415 мкм, соответственно (Рис. 5). Наконечник RFT2 вставляется на 1 мм короче рабочего длины, требуя размеров подготовки канала ISO 30 или больше, в то время как наконечник RFT3 вставляется до соединения средней и апикальной третьей, требуя размеров канала ISO 45 или больше. Эти размеры хорошо соответствуют типичным размерам рабочей ширины, подготовленным с помощью файлов LSX. Внутриканальная лазерная терапия выполняется в две фазы: Фаза очистки для удаления смывного слоя и остатков, и Фаза дезинфекции для абляции тканей и уничтожения бактерий.

Этап очистки (1.25 Вт; 50 Гц; 24 % воздух; 30 % вода)
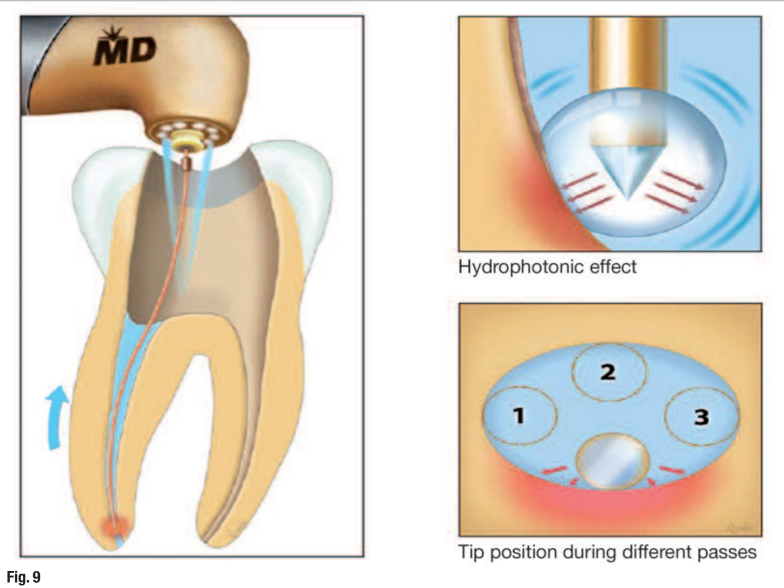
Этот этап использует воду и удаляет смывной слой и мусор без использования химических ирригантов. Он занимает от двух до трех минут на канал и использует гидро-фотонику для создания мощного микро-агитационного эффекта по всей системе канала.
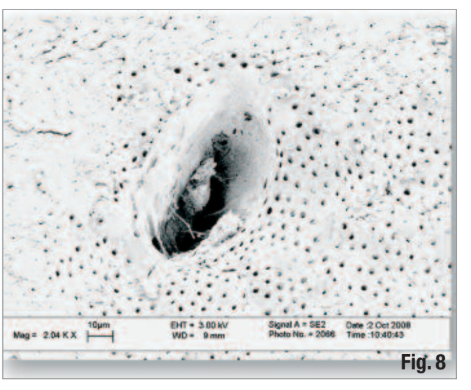
Общепринято, что удаление смывного слоя облегчает очистку и дезинфекцию дентинных канальцев и улучшает герметизацию корневого канала. При объединении результатов двух исследований, Er,Cr:YSGG с радиальными насадками обеспечивал значительно лучшее удаление смывного слоя в апикальной, средней и корональной третях по сравнению с двумя ротационными техниками. Это чрезвычайно эффективное действие открывает дентинные канальцы, боковые каналы и истмусы в подготовке к дезинфекции (Рис. 6–8).


Техника очистки после завершения доступа, подготовки рабочей ширины и ирригации с отрицательным давлением:
- используйте RFT2 для выполнения очистки апикальной и частичной корональной двух третей;
- выберите рекомендуемые настройки лазера в мокром режиме;
- наполните канал стерильным раствором;
- вставьте наконечник RFT2 на 1 мм короче рабочего длины;
- активируйте лазер при извлечении наконечника коронально со скоростью примерно 1 мм/с и поддерживайте наконечник в контакте с боковой поверхностью стенки канала на протяжении всего прохода от апекса к корональной части;
- повторите шаги 4 и 5 один или два раза, чтобы убедиться, что весь внутренний канал был очищен (Рис. 9);
- поместите наконечник RFT3 в ручку для выполнения окончательной очистки корональной двух третей;
- наполните канал стерильным раствором;
- вставьте наконечник в соединение апикальной и средней трети корневого канала; и
- повторите шаги 5 и 6.
Фаза дезинфекции (0.75 Вт; 20 Гц; 10 %воздуха; 0 %воды)
Как уже упоминалось, лазерная энергия, излучаемая лазером Er,Cr:YSGG, высоко поглощается водой в тканях и микроорганизмах, что приводит к мгновенной фотоабляции. Кроме того, возникающее микропульсовое расширение и коллапс внутритрубочной воды создают акустические волны, достаточно сильные, чтобы разрушить и уничтожить внутритрубочные бактерии. Этот эффект наиболее эффективен в сухом режиме, так как лазерная энергия не поглощается водяным распылением и может оказать свое полное воздействие на бактерии. Это было подтверждено Гордоном и др., которые достигли 99.7 % уровня уничтожения E. faecalis в сухом режиме. Техника для фазы дезинфекции такая же, как и для фазы очистки, но с другими настройками лазера в сухом режиме.
Клинические применения
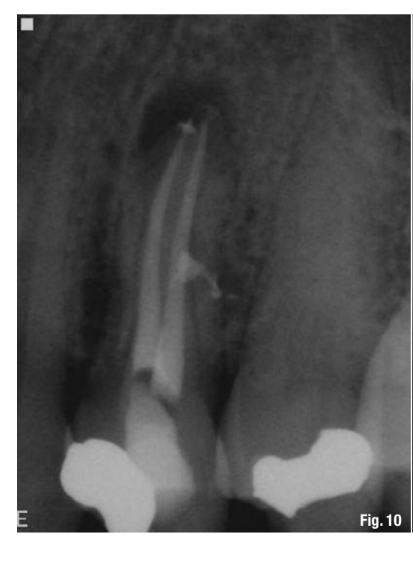
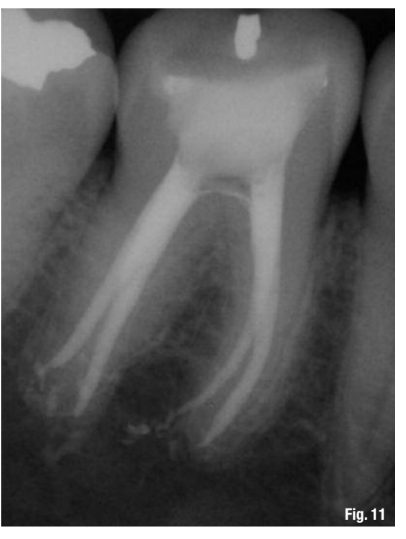
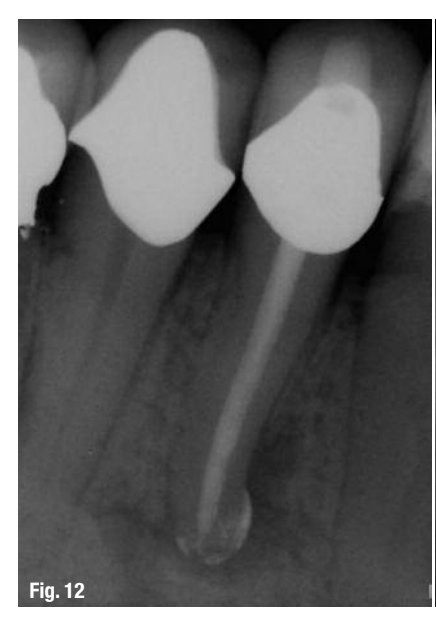
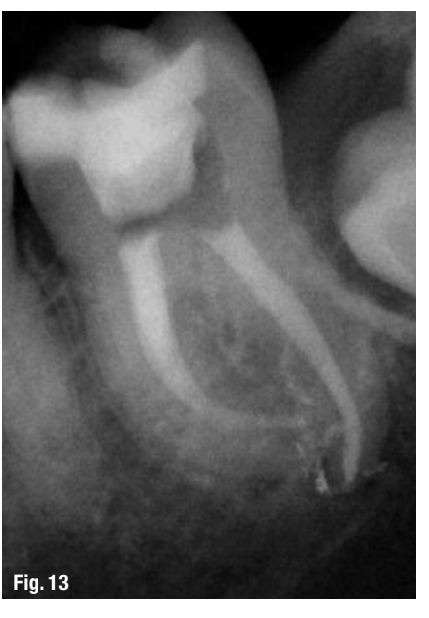
Хотя этот протокол рекомендуется для всех эндодонтических процедур (Рис. 10–13), он наиболее ценен в следующих клинических ситуациях:
- инфицированные случаи с апикальными, латеральными и/или фуркальными радиолюценциями;
- повторные лечения с периапикальным периодонтитом;
- остро воспаленные случаи, особенно те, которые диагностированы с синдромом треснувшего зуба;
- внутреннее и внешнее резорбция;
- постоянные инфекции, не поддающиеся традиционному эндодонтическому лечению; и
- необъяснимый, длительный послеоперационный дискомфорт.
Резюме
Описан протокол очистки, формовки и дезинфекции корневых каналов, который максимизирует удаление тканей, мусора, смывного слоя и бактерий из систем корневых каналов. Используя комбинацию управления рабочей шириной с инструментами LightSpeed LSX, ирригацию с высоким объемом апикального отрицательного давления и эвакуацию с системой EndoVac, а также внутриконтурную лазерную терапию с радиальными наконечниками с использованием лазера WaterlaseMD, возможность устранения бактерий из инфицированных систем корневых каналов может вскоре стать реальностью.
Ссылки:
- Siqueira JF, Rocas IN: Клинические последствия и микробиология бактериальной устойчивости после процедур лечения. J Endod. 2008;34(11):1291–1301.
- Gordon W, Atabakhsh VA, Meza F, Doms A, Nissan R, Rizoiu I, Stevens R: Антимикробная эффективность лазера эрбия, хрома: иттрия-скандия-галлия-граната с радиальными насадками на стенках корневых каналов, инфицированных Enterococcus faecalis. JADA. 2007;138(7):992–1002.
- Kouchi Y, Ninomiya J, Yasuda H, Fukui K, Moriyama T, Okamoto H: Расположение Streptococcus mutans в дентинных канальцах открытых инфицированных корневых каналов. J Dent Res. 1980;59:2038–46.
- Haapasalo M, Orstavik D: Инфекция и дезинфекция дентинных канальцев in vitro. J Dent Res. 1987;66(8):1375–9.
- Berutti E, Marini R, Angeretti A: Способность различных ирригантов проникать в дентинные канальцы. J Endod. 1997;23:725–7.
- Zou L, Shen Y, Li W, Haapasalo M: Проникновение гипохлорита натрия в дентин. J Endod. 2010;36(5):793–6.
- Schoop U, Barylyak A, Goharkhay K, Beer F, Wernisch J, Georgopoulos A, Sperr W, Moritz A: Влияние лазера нербия, хрома: иттрия-скандия-галлия-граната с радиальными насадками на эндодонтическое лечение. Lasers Med Sci. 2007;24(1):59–65.
- Allen F: Исследование in vivo очистки апекса. General Dentistry. 2007;449–56.
- Kerekes K, Tronstad L: Морфометрические наблюдения за корневыми каналами человеческих моляров. J Endod. 1977;3:114–8.
- Wu MK, R’oris A, Barkis D, Wesselink P: Распространенность и протяженность длинных овальных каналов в апикальной трети. OOO. 2000;89(6):739–43.
- Chow TW: Механическая эффективность ирригации корневых каналов. J Endod. 1983;9(11):475–8.
- Tay FR, Gu L, Schoeffel GL, Wimmer C, Susin L, Zhang K, Arun SN, Kim J, Looney JW, Pashley DJ: Влияние парового замка на дебридмент корневого канала с использованием иглы с боковым вентиляцией для доставки ирриганта под положительным давлением. J Endod. 2010;36(4):745–50.
- Schoeffel J: Метод EndoVac для эндодонтической ирригации, Часть 2–Эффективность. Dentistry Today. 2008;27(1).
- Nielsen BA, Baumgartner JC: Сравнение системы EndoVac с игольной ирригацией корневых каналов. J Endod. 2007;33(5):611–5.
- Prashanth VS: Оценка новой системы ирригации корневых каналов по сравнению с традиционной: Экспериментальное исследование. Discus Dental, Culver City, CA: The EndoFiles Newsletter. 2008.
- Sung E, Rankin DD, Rizoiu I, Chueh P: Технология Biolase. неопубликованное исследование. 2008.
- Peters O, Barbakow F: Влияние ирригации на остатки и слой налета на стенках канала: Исследование с использованием сканирующей электронной микроскопии. J Endod. 2000;26(1):6–10.